
【題目】下列說法錯誤的是( )
A. ![]() 、
、![]() 、H+和H2是氫元素的四種不同粒子
、H+和H2是氫元素的四種不同粒子
B. ![]() 和
和 ![]() 、石墨和金剛石均為同素異形體
、石墨和金剛石均為同素異形體
C. 1H和2H是不同的核素
D. 12C和14C互為同位素,物理性質不同,但化學性質幾乎完全相同
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】在密閉容器中發生下列反應:I2(g)+H2(g)![]() 2HI(g)(正反應為放熱反應)。起始時,n(H2)=a mol,n(I2)=b mol。只改變表中列出的條件,其他條件不變,試將化學反應速率的改變填入相關的表格中(填“增大”“減小”或“不變”)。
2HI(g)(正反應為放熱反應)。起始時,n(H2)=a mol,n(I2)=b mol。只改變表中列出的條件,其他條件不變,試將化學反應速率的改變填入相關的表格中(填“增大”“減小”或“不變”)。
編號 | 改變的條件 | 反應速率 |
(1) | 升高溫度 | ______ |
(2) | 加入正催化劑 | ______ |
(3) | 再充入a mol H2 | ______ |
(4) | 將容器的容積擴大到原來的2倍 | ______ |
(5) | 保持容積不變,通入b mol Ne | ______ |
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA是阿伏加德羅常數的值,下列說法正確的是
A. 常溫常壓下,6.4g O2和O3的混合氣體中含有的分子數為0.4 NA
B. 標準狀況下,2.24 L CCl4分子中共價鍵的數目為0.4NA
C. 25℃時,pH=13的Ba(OH)2溶液中含有氫氧根離子數為0.1 NA
D. 高溫下,16.8 g Fe與足量水蒸氣完全反應失去0.8NA個電子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】元素A位于第4周期,其基態原子有6個未成對電子;元素B的原子最外層電子數是其內層電子總數的3倍;元素C基態原子的3p軌道上有4個電子,元素D是有機物必不可少的中心元素,E是周期表中原子半徑最小的元素。
(1)元素B與元素C可形成多種化合物。
①元素B與C中電負性較大的是______(填元素符號)。
②離子CB42—的空間構型為______(用文字描述)。
(2)B和E形成簡單化合物的沸點大于C和E形成的簡單化合物,其原因______。
(3)含A3+的溶液與NaCl、氨水反應可得到化合物Na[A(NH3)2Cl4]。
①基態A原子的電子排布式是______。
②1 mol配合物Na[A(NH3)2Cl4]中含σ鍵的數目為______mol。
(4)下圖為B、D、E三種元素形成的一種化合物的球棍模型,推測該化合物中D原子的雜化方式______。
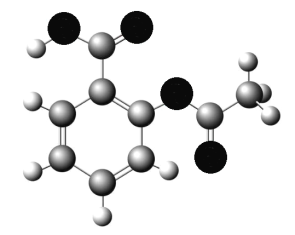
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】福酚美克是一種影響機體免疫力功能的藥物,可通過以下方法合成:
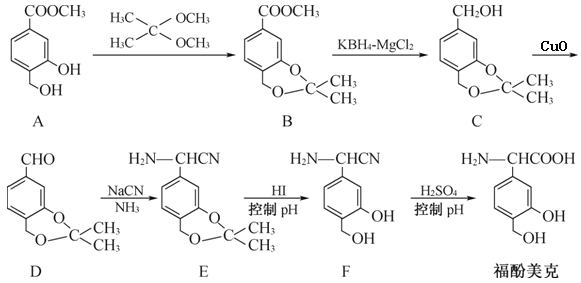
(1)A中的含氧官能團有____和____(填名稱)。
(2)寫出C→D的轉化的化學方程式____,該反應屬于____(填反應類型)。
(3)流程中設置A→B、E→F的目的是____。
(4)A的一種同分異構體X滿足下列條件:
① X分子中有4種不同化學環境的氫
② X能與FeCl3溶液發生顯色反應
③ 1 mol X最多能與4 mol NaOH發生反應
寫出該同分異構體的結構簡式:____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述中,不能用勒夏特列原理解釋的是
A. 紅棕色的NO2,加壓后顏色先變深后變淺
B. 高壓比常壓有利于合成SO3的反應
C. 加入催化劑有利于氨的合成
D. 工業制取金屬鉀Na(l)+KCl(l)![]() NaCl(l)+K(g)選取適宜的溫度,使K變成蒸氣從反應混合物中分離出來
NaCl(l)+K(g)選取適宜的溫度,使K變成蒸氣從反應混合物中分離出來
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組離子在相應的條件下可能大量共存的是( )
A. 能使pH試紙變紅的溶液中:CO32—、K+、Cl-、Na+
B. 由水電離產生的c(OH-)=1×10-10mol·L-1的溶液中:NO3—、Mg2+、Na+、SO42—
C. 在![]() =1×1012的溶液中:NH4+、Fe2+、Cl-、NO3—
=1×1012的溶液中:NH4+、Fe2+、Cl-、NO3—
D. ![]() =10-14mol·L-1的溶液中:Na+、HCO3—、Cl-、K+
=10-14mol·L-1的溶液中:Na+、HCO3—、Cl-、K+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】過氧化鈣(CaO2)是一種白色晶體,無臭無味,能潮解,難溶于水,可與水緩慢反應;不溶于醇類、乙醚等,易與酸反應,常用作殺菌劑、防腐劑等。通常利用CaCl2在堿性條件下與H2O2反應制得。
某化學興趣小組在實驗室制備CaO2的實驗方案和裝置示意圖(圖一)如下:


請回答下列問題:
(1)三頸燒瓶中發生的主要反應的化學方程式為___________________________________;
(2)支管B的作用是_________________________;
(3)步驟③中洗滌CaO2·8H2O的液體X的最佳選擇是____________;
A.無水乙醇 B.濃鹽酸 C.水 D.CaCl2溶液
(4)過氧化鈣可用于長途運輸魚苗,這體現了過氧化鈣___________的性質;
A.可緩慢供氧 B.能吸收魚苗呼出的CO2氣體 C.能潮解 D.可抑菌
(5)已知CaO2在350℃時能迅速分解,生成CaO和O2。該小組采用如圖二所示的裝置測定剛才制備的產品中CaO2的純度(設雜質不分解產生氣體)
①檢查該裝置氣密性的方法是:_________________________________;
②使用________(填儀器名稱)準確稱取0.5000g樣品,置于試管中加熱使其完全分解,收集到33.60mL(已換算為標準狀況)氣體,則產品中過氧化鈣的質量分數為________(保留4位有效數字);
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】反應4A(g)+5B(g)![]() 4C(g)+6D(g) 在5 L的密閉容器中進行反應,30 min后,C的物質的量增加了 0.30 mol。下列敘述正確的是( )
4C(g)+6D(g) 在5 L的密閉容器中進行反應,30 min后,C的物質的量增加了 0.30 mol。下列敘述正確的是( )
A. 30 min中A的平均反應速率是0.010 mol·L-1·min-1
B. 容器中D的物質的量一定增加了0.45 mol
C. 容器中A、B、C、D的物質的量之比一定是4∶5∶4∶6
D. 容器中A的物質的量一定增加0.30 mol
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com