
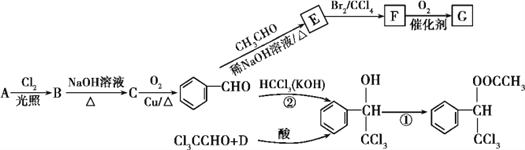
【題目】香料甲和G都在生活中有很多用途,其合成路線如下:
已知:①R1—CHO+R2—CH2—CHO![]()
![]() (R1、R2代表烴基或氫原子)
(R1、R2代表烴基或氫原子)
②D與A互為同系物;在相同條件下,D蒸氣相對于氫氣的密度為39。
(1)A的名稱是____,G中含氧官能團的名稱是____。
(2)②的反應類型是____,B和F的結構簡式分別為______、______。
(3)寫出一種能鑒別A和D的試劑:______;C有多種同分異構體,其中屬于芳香族化合物的有____種。
(4)寫出反應①的化學方程式:_____________。
(5)G的同分異構體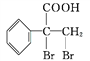 是一種重要的藥物中間體,其合成路線與G相似,請以
是一種重要的藥物中間體,其合成路線與G相似,請以![]() 為原料設計它的合成路線(其他所需原料自選)_________。
為原料設計它的合成路線(其他所需原料自選)_________。
【答案】 甲苯 羧基 加成反應 ![]()
![]() 酸性高錳酸鉀溶液 4
酸性高錳酸鉀溶液 4 ![]() +CH3COOH
+CH3COOH![]()
![]() +H2O
+H2O 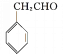
![]()
![]()
![]()
![]()
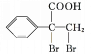
【解析】由C→![]() 及反應條件可知C為苯甲醇,B為
及反應條件可知C為苯甲醇,B為![]() ,A為甲苯。在相同條件下,D的蒸氣相對于氫氣的密度為39,則D的相對分子質量為39×2=78,D與A互為同系物,由此知D為芳香烴,設1個D分子中含有n個碳原子,則有14n-6=78,解得n=6,故D為苯;
,A為甲苯。在相同條件下,D的蒸氣相對于氫氣的密度為39,則D的相對分子質量為39×2=78,D與A互為同系物,由此知D為芳香烴,設1個D分子中含有n個碳原子,則有14n-6=78,解得n=6,故D為苯;![]() 與乙醛反應得到E,結合信息①,E為
與乙醛反應得到E,結合信息①,E為![]() ,E與溴發生加成反應得到的F為
,E與溴發生加成反應得到的F為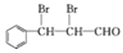 ,F發生氧化反應生成的G為
,F發生氧化反應生成的G為![]() 。
。
(1)根據分析可知,A為甲苯,G為![]() ,則G中含氧官能團為羧基,故答案為:甲苯; 羧基;
,則G中含氧官能團為羧基,故答案為:甲苯; 羧基;
(2)反應②為苯甲醛與氯仿發生加成反應生成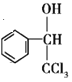 ,根據上述分析,B和F的結構簡式分別為
,根據上述分析,B和F的結構簡式分別為![]() 、
、![]() ,故答案為:加成反應;
,故答案為:加成反應;![]() ;
;![]() ;
;
(3)甲苯能使酸性高錳酸鉀溶液褪色,而苯不能;C為苯甲醇屬于芳香族化合物的苯甲醇的同異構體有鄰甲基苯酚、間甲基苯酚、對甲基苯酚和苯甲醚(![]() ),共4種,故答案為:酸性高錳酸鉀溶液;4;
),共4種,故答案為:酸性高錳酸鉀溶液;4;
(4)反應①為乙酸和![]() 發生酯化反應,化學方程式為
發生酯化反應,化學方程式為![]() +CH3COOH
+CH3COOH![]()
![]() +H2O,故答案為:
+H2O,故答案為:![]() +CH3COOH
+CH3COOH![]()
![]() +H2O;
+H2O;
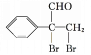
(5)苯乙醛與甲醛反應生成![]() ,
,![]() 再與溴發生加成反應生成
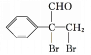
再與溴發生加成反應生成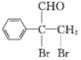 ,最后
,最后 發生催化氧化反應生成
發生催化氧化反應生成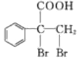 ,故合成路線為
,故合成路線為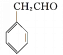
![]()
![]()
![]()
![]()
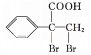 ,故答案為:
,故答案為:
![]()
![]()
![]()

![]()
 。
。


 華東師大版一課一練系列答案
華東師大版一課一練系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化學 來源: 題型:
【題目】請回答下列問題:
(1)某元素X基態原子的最外層有3個未成對電子,次外層有2個電子,其價電子排布圖為___,其原子核外有___種不同運動狀態的電子;其最低價氫化物電子式為___,中心原子采用___雜化,分子立體構型為___。
(2)某元素Y基態原子的M層全充滿,N層沒有成對電子,只有一個未成對電子,其元素名稱為___,Y+的外圍電子排布式為___,該元素固體單質常常采用___堆積方式,配位數為___,空間利用率為___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在處理廢水時某反應體系中有6種粒子:N2、HCO3-、ClO-、CNO-、H2O、Cl-,在反應過程中部分離子濃度與反應進程關系如圖所示。下列有關該反應的說法正確的是( )

A. 在上述反應體系中,CNO-是氧化劑
B. 還原產物與氧化產物的物質的量之比為1∶3
C. 在標準狀況下,產生4.48 L N2時轉移0.8 mol電子
D. 上述反應中,只有兩種元素化合價發生了變化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某研究小組利用軟錳礦![]() 主要成分為
主要成分為![]() ,另含少量鐵,鈣,銅等金屬化合物
,另含少量鐵,鈣,銅等金屬化合物![]() 作脫硫劑,通過如下簡化流程,既脫除燃煤尾氣中的
作脫硫劑,通過如下簡化流程,既脫除燃煤尾氣中的![]() ,又制得電池材料
,又制得電池材料![]() 反應條件已省略
反應條件已省略![]()
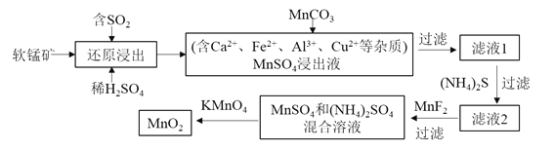
請回答下列問題:
![]() 上述還原浸出是脫硫過程,實現了 ______
上述還原浸出是脫硫過程,實現了 ______ ![]() 選填編號
選填編號![]() .
.
![]() 廢氣物的綜合利用
廢氣物的綜合利用
![]() 臭氧層空洞的減少
臭氧層空洞的減少
![]() 白色污染的減少
白色污染的減少
![]() 酸雨的減少
酸雨的減少
![]() 寫出上述軟錳礦經還原浸出生成
寫出上述軟錳礦經還原浸出生成![]() 的化學方程式是 ______ .
的化學方程式是 ______ .
![]() 用
用![]() 能除去還原浸出液中的
能除去還原浸出液中的![]() ,請用離子方程式解釋其原因是 ______ .
,請用離子方程式解釋其原因是 ______ .
![]() 加入
加入![]() 的目的主要是除去 ______ ;加入
的目的主要是除去 ______ ;加入![]() 的目的主要是除去 ______ ;
的目的主要是除去 ______ ;![]() 填離子符號
填離子符號![]()
![]() 下列各組試劑中,能準確測定一定體積燃煤尾氣中
下列各組試劑中,能準確測定一定體積燃煤尾氣中![]() 含量的是 ______
含量的是 ______ ![]() 填編號
填編號![]()
a.NaOH溶液、石蕊試液
b.稀![]() 酸化的
酸化的![]() 溶液
溶液
c.碘水、淀粉溶液
d.氨水、石蕊試液
![]() 用電化學法模擬工業處理
用電化學法模擬工業處理![]() 將硫酸工業尾氣中的
將硫酸工業尾氣中的![]() 通入如圖裝置
通入如圖裝置![]() 電均為惰性材料
電均為惰性材料![]() 進行實驗,可用于制備硫酸,同時獲得電能:
進行實驗,可用于制備硫酸,同時獲得電能:
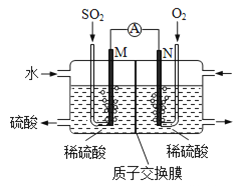
![]() 極發生的電極反應式為 ______ .
極發生的電極反應式為 ______ .
![]() 若使該裝置的電流強度達到
若使該裝置的電流強度達到![]() ,理論上每分鐘應向負極通入標準狀況下氣體的體積為 ______
,理論上每分鐘應向負極通入標準狀況下氣體的體積為 ______ ![]() 保留3位小數,已知:1個
保留3位小數,已知:1個![]() 所帶電量為
所帶電量為![]() .
.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)4個碳原子間均以單鍵結合的方式有4種,請在下面的方框中補充另外3種結合方式:________________

(2)寫出碳原子數為5的烷烴的同分異構體的結構簡式______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在恒容密閉容器中,可逆反應C(s)+CO2(g)![]() 2CO(g),達到平衡狀態的標志是
2CO(g),達到平衡狀態的標志是
A. 單位時間內生成nmolCO2的同時生成2nmolCO
B. 單位時間內生成nmolCO2的同時生成nmolC
C. 混合氣體的密度不再改變的狀態
D. 混合氣體的壓強不再改變的狀態
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列根據實驗操作和現象所得出的結論正確的是( )
選項 | 實驗操作 | 實驗現象 | 結論 |
A | 等體積 | 相同時間內 |
|
B | 將濕潤的淀粉- | 試紙只在 | 氧化性: |
C | 將光亮的鎂條放入盛有 | 有大量氣泡產生 | 生成的氣體是 |
D | 向NaHCO3溶液中加入NaAlO2溶液 | 有白色沉淀生成 |
|
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(化學——選修2:化學與技術)
甲酸鈉廣泛用作催化劑、穩定合成劑、印染行業的還原劑,還可用于生產保險粉、草酸和甲酸。甲酸鈉用電石爐廢氣(75%~90% CO,以及少量CO2、H2S、N2、CH4等)合成,其合成部分工藝流程如圖:
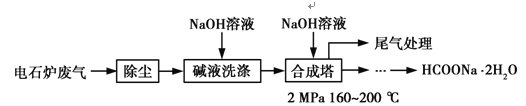
(1)上述工藝用堿液洗滌的目的是___________,可能發生的反應有______________(寫兩個化學方程式)。
(2)上述合成工藝中采用循環噴射吸收合成,其目的是_______________;最后尾氣主要成分是__________________。
(3)甲酸鈉高溫時分解制取草酸鈉(Na2C2O4)的化學方程式為__________________。
(4)在甲酸鈉、氫氧化鈉混合溶液中通入二氧化硫氣體,可得到重要的工業產品保險粉(Na2S2O4),同時產生二氧化碳氣體,該反應的離子方程式為___________________。
(5)某廠測知合成塔中甲酸鈉生產產率為40%,要制得溶質質量分數為5%的HCOONa溶液1噸,需要CO在標況下的體積為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】最近浙江大學成功研制出具有較高能量密度的新型鋁一石墨烯(Cn)電池(如圖)。該電池分別以鋁、石墨烯為電極,放電時電池中導電離子的種類不變。已知能量密度=電池容量(J)÷負極質量(g)。下列分析正確的是
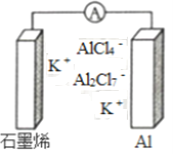
A. 放電時,Cn(石墨烯)為負極
B. 放電時,Al2Cl7-在負極轉化為AlCl4-
C. 充電時,陽極反應為4 Al2Cl7-+3e-=A1+7AlCl4-
D. 以輕金屬為負極有利于提高電池的能量密度
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com