
【題目】有A、B、C、D、E五種短周期主族元素,原子序數由A到E逐漸增大.①A元素最外層電子數是次外層電子數的2倍. ②B的陰離子和C的陽離子與氖原子的電子層結構相同.③在通常狀況下,B的單質是氣體,0.1molB的氣體與足量的氫氣完全反應共有0.4mol電子轉移.④C的單質在點燃時與B的單質充分反應,生成淡黃色的固體,此淡黃色固體能與AB2反應可生成B的單質.⑤D的氣態氫化物與其最高價含氧酸間能發生氧化還原反應.請寫出:
(1)A元素的最高價氧化物的電子式 _________________________ .
(2)B元素在周期表中的位置 _______________________________ .
(3)B單質與C單質在點燃時反應的生成物中所含化學鍵類型有 ____________________ .
(4)D元素的低價氧化物與E的單質的水溶液反應的化學方程式為 ______________ .
(5)元素D與元素E相比,非金屬性較強的是 ______ (用元素符號表示),下列表述中能證明這一事實的是 _______________ (填選項序號).
a.常溫下D的單質和E的單質狀態不同
b.E的氫化物比D的氫化物穩定
c.一定條件下D和E的單質都能與鈉反應
d.D的最高價含氧酸酸性弱于E的最高價含氧酸
e.D的單質能與E的氫化物反應生成E單質.
【答案】 ![]() 第二周期ⅥA族 離子鍵、共價鍵 SO2+Cl2+2H2O=H2SO4+2HCl Cl bd
第二周期ⅥA族 離子鍵、共價鍵 SO2+Cl2+2H2O=H2SO4+2HCl Cl bd
【解析】有A、B、C、D、E五種短周期主族元素,原子序數由A到E逐漸增大。A的最外層電子數是次外層電子數的2倍,則A原子有2個電子層,最外層電子數為4,則A為碳元素;B的陰離子和C的陽離子與氖原子的電子層結構相同,則C處于第三周期,B處于第二周期,在通常狀況下,B的單質是氣體,0.1molB的氣體與足量的氫氣完全反應共有0.4mol電子轉移,B元素表現-2價,則B為O元素;C的單質在點燃時與B的單質充分反應,生成淡黃色的固體,此淡黃色固體能與AB2反應可生成B的單質,則C為Na;D的氣態氫化物與其最高價含氧酸間能發生氧化還原反應,E的原子序數最大,則D為S元素,E為Cl,據此解答。
詳解: (1)A為碳元素,最高價氧化物為CO2,電子式為![]() ,因此,本題正確答案是:
,因此,本題正確答案是: ![]() ;
;
(2)B為氧元素,在周期表中的位置:第二周期VIA族,因此,本題正確答案是:第二周期VIA族;
(3)B單質與C單質在點燃時反應的生成物為Na2O2,含有離子鍵、共價鍵,因此,本題正確答案是:離子鍵、共價鍵;
(4)D元素的低價氧化物為二氧化硫,與氯氣的水溶液反應的離子方程式為SO2+Cl2+2H2O=H2SO4+2HCl,
因此,本題正確答案是: SO2+Cl2+2H2O=H2SO4+2HCl;
(5)同周期自左而右元素非金屬性增強,故非金屬性Cl>S,
a.單質狀態屬于物理性質,不能比較元素非金屬性,故a錯誤;
b.氫化物穩定性與元素非金屬性一致,氯化氫比硫化氫穩定,說明氯的非金屬性更強,故b正確;
c.與變價金屬反應可以根據產物中金屬化合價判斷非金屬元素的非金屬性強弱,Na不是變價金屬,不能判斷硫與氯的非金屬性強弱,故c錯誤;
d.最高價含氧酸的酸性與中心元素的非金屬性一致,故d正確;
e.硫不能與HCl反應生成氯氣,故e錯誤。
因此,本題正確答案是:Cl;bd。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】有機物CH3—CH=CHCl能發生的反應有( )
①取代反應 ②加成反應 ③消去反應 ④使酸性KMnO4溶液褪色 ⑤與AgNO3溶液反應生成白色沉淀 ⑥聚合反應
A. 以上反應均能發生 B. 只有⑥不能發生 C. 只有⑤不能發生 D. 只有②不能發生
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學家格哈德·埃特爾證實了氫氣與氮氣在固體催化劑表面合成氨的反應過程,示意圖如下:

![]()
下列關于合成氨反應的敘述中不正確的是
A. 該過程表明,在化學反應中存在化學鍵的斷裂與形成
B. 在催化劑的作用下,反應物的化學鍵變得容易斷裂
C. 過程②需吸收能量,過程③則放出能量
D. 常溫下該反應難以進行,是因為常溫下生成物的化學鍵難以形成
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】熱激活電池可用作火箭、導彈的工作電源。一種熱激活電池的基本結構如圖所示,其中作為電解質的無水LiCl-KCl混合物受熱熔融后,電池即可瞬間輸出電能。該電池總反應為:PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb ,下列說法不正確的是( )

A. 工作時,電池的正極質量逐漸減輕
B. 放電過程中,Li+向正極移動
C. 每轉移0.1 mol電子,理論上生成20.7 g Pb
D. 常溫時,在正負極間接上電流表,指針不偏轉
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列溶液中通入足量SO2,根據其實驗現象,所得結論不正確的是
溶液 | 現象 | 結論 | |
A | 含HCl、BaCl2和FeCl3的溶液 | 產生白色沉淀 | SO2有還原性 |
B | H2S溶液 | 產生黃色沉淀 | SO2有氧化性 |
C | 酸性KMnO4溶液 | 紫紅色溶液褪色 | SO2有漂白性 |
D | 加有酚酞的NaOH溶液 | 褪色 | SO2是酸性氧化物 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期元素A、B、C、D、E在元素周期表中的位置如下圖所示,其中B元素是碳元素。請回答下列問題:
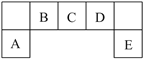
(1)B元素在周期表中的位置:_________________;請寫出該原子的電子式:___________;其原子核外電子能量最高的能級是:_______。
(2)比較A、C、D元素簡單離子半徑的大小:_______>_______>_______ (填微粒符號)。
(3)F與D同主族且相鄰,請比較D的氫化物和F的氫化物穩定性大小:_______ (用化學式表示)。
(4)E單質常用濕潤的淀粉碘化鉀試紙檢驗。有學生對淀粉碘化鉀進行了實驗探究。在淀粉碘化鉀溶液中,滴加少量次氯酸鈉溶液,立刻會看到溶液變藍色,這是因為_______(請結合氧化還原反應知識解釋相關現象,下同)。在所形成的藍色溶液中,再滴加亞硫酸鈉溶液,發現藍色逐漸消失,這是因為_________________。據此分析,I2、ClO-、SO42-氧化性有弱到強的順序排列為____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】海洋資源的利用具有廣闊前景。
(1)無需經過化學變化就能從海水中獲得的物質是________(填序號)。
A.Cl2 B.淡水 C.燒堿 D.粗鹽
(2)下圖是從海水中提取鎂的簡單流程。

①工業上常用于沉淀Mg2+的試劑A是________,轉Mg(OH)2化為MgCl2的離子方程式是____________。
②由無水MgCl2制取Mg的化學方程式是________________________。
(3)海帶灰中富含以I-形式存在的碘元素。實驗室提取I2的途徑如下所示:
![]()
①灼燒海帶時所用的主要儀器名稱是________________。
②向酸化的濾液中加H2O2溶液,寫出該反應的離子方程式_______________________。
反應結束后,再加入CCl4作萃取劑,振蕩、靜置,可以觀察到CCl4層呈________色。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】H2S是一種劇毒氣體,如圖為質子膜H2S燃料電池的示意圖,可對H2S廢氣資源化利用。下列敘述錯誤的是

![]()
A. a是負極,電池工作時,電子的流動力向是:電極a-負載一電極b-質子膜一電極a
B. 電池工作時,化學能轉化為電能和熱能
C. 電極b上發生的電極反應式為O2+ 4e-+4H+=2H2O
D. 當電路中通過4mol電子時,有4molH+經質子膜進入正極區
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關化學用語表示正確的是( )
A. 乙酸的結構簡式:C2H4O2
B. NH3的電子式:![]()
C. 離子結構示意圖![]() 可以表示32S2-,又可以表示34S2-
可以表示32S2-,又可以表示34S2-
D. 比例模型![]() 可以表示甲烷分子,也可以表示四氯化碳分子
可以表示甲烷分子,也可以表示四氯化碳分子
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com