


科目:高中化學 來源: 題型:
 在化學反應中,只有極少數能量比平均能量高得多的反應物分子發生碰撞時才能發生化學反應.能引發化學反應的碰撞稱之為有效碰撞,這些分子稱為活化分子.使普通分子變成活化分子所需提供的最低限度的能量叫活化能,其單位用kJ?mol-1表示.請認真觀察下圖,然后回答問題.
在化學反應中,只有極少數能量比平均能量高得多的反應物分子發生碰撞時才能發生化學反應.能引發化學反應的碰撞稱之為有效碰撞,這些分子稱為活化分子.使普通分子變成活化分子所需提供的最低限度的能量叫活化能,其單位用kJ?mol-1表示.請認真觀察下圖,然后回答問題.| 1 | 2 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
| 高溫 |
| 溫度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常數K | 10 | 9 | 1 | 0.6 |
查看答案和解析>>
科目:高中化學 來源: 題型:
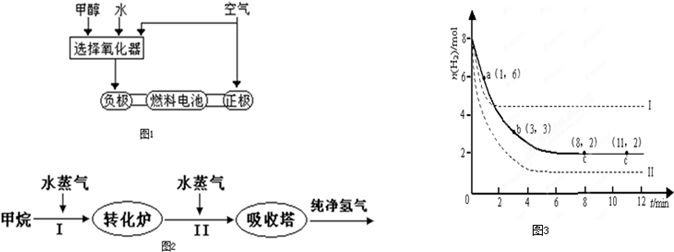
 能源是人類生存和發展的重要支柱.研究和有效地開發新能源在能源緊缺的今天具有重要的理論意義.
能源是人類生存和發展的重要支柱.研究和有效地開發新能源在能源緊缺的今天具有重要的理論意義.| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
 在化學反應中,能引發化學反應的分子間碰撞稱之為有效碰撞,這些分子稱為活化分子.使普通分子變成活化分子所需提供的最低能量叫活化能,其單位用kJ?mol-1表示.請認真觀察圖,然后回答問題.
在化學反應中,能引發化學反應的分子間碰撞稱之為有效碰撞,這些分子稱為活化分子.使普通分子變成活化分子所需提供的最低能量叫活化能,其單位用kJ?mol-1表示.請認真觀察圖,然后回答問題.| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
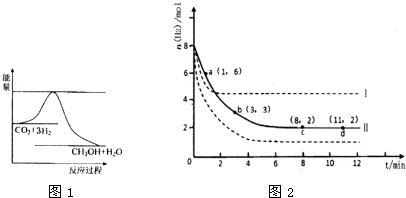
| 1 | 2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com