
【題目】A~G都是有機化合物,它們的轉化關系如下:
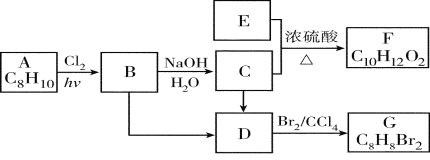
請回答下列問題:
(1)已知:6.0 g化合物E完全燃燒生成8.8 g CO2和3.6 g H2O;E的蒸氣與氫氣的相對密度為30,則E的分子式為________;
(2)A為一取代芳烴,B中含有一個甲基。由B生成C的化學方程式為:________________;
(3)由B生成D的反應條件是________________;
(4)在G的同分異構體中,苯環上一硝化的產物只有一種的共有________個,其中核磁共振氫譜有兩組峰,且峰面積比為1∶1的是_________(填結構簡式)。
【答案】C2H4O2 ![]()
![]() 氫氧化鈉的醇溶液,加熱 7
氫氧化鈉的醇溶液,加熱 7 
【解析】
E的蒸氣與氫氣的相對密度為30,則Mr(E)=30![]() 2=60,6.0 gE的物質的量是0.1mol,完全燃燒后生成CO2和H2O的物質的量分別為
2=60,6.0 gE的物質的量是0.1mol,完全燃燒后生成CO2和H2O的物質的量分別為![]() =0.2mol,
=0.2mol,![]() =0.2mol,分子中N(C)=
=0.2mol,分子中N(C)=![]() =2、N(H)=
=2、N(H)=![]() =4,故N(O)=
=4,故N(O)=![]() =2,故E的分子式是C2H4O2。
=2,故E的分子式是C2H4O2。
A為一取代芳烴,由分子式可以知道為苯的同系物,故A為![]() ,A與氯氣在光照條件下發生取代反應生成B,而B中含有一個甲基,則B為
,A與氯氣在光照條件下發生取代反應生成B,而B中含有一個甲基,則B為![]() ,B發生水解反應生成C為
,B發生水解反應生成C為![]() ,C與E發生酯化反應生成F,結合F的分子式可以知道,應是發生酯化反應,則E為CH3COOH,F為
,C與E發生酯化反應生成F,結合F的分子式可以知道,應是發生酯化反應,則E為CH3COOH,F為![]() ,B、C轉化都得到D,D與溴發生加成反應生成G,則B、C均發生消去反應生成D,故D為
,B、C轉化都得到D,D與溴發生加成反應生成G,則B、C均發生消去反應生成D,故D為![]() ,則G為
,則G為![]() ,據此解答。
,據此解答。
(1)由上述分析可以知道,E的分子式為C2H4O2,
因此,本題正確答案是:C2H4O2;
(2)由B生成C的化學方程式為![]() ,
,
因此,本題正確答案是:![]() ;
;
(3)由B生成D是![]() 發生消去反應生成
發生消去反應生成![]() ,反應條件為:氫氧化鈉醇溶液、加熱,
,反應條件為:氫氧化鈉醇溶液、加熱,
因此,本題正確答案是:氫氧化鈉的醇溶液,加熱;
(4)在G(![]() )的同分異構體中,苯環上一硝化的產物只有一種,對稱性高,可以含有2個相同的取代基,且處于對位,為
)的同分異構體中,苯環上一硝化的產物只有一種,對稱性高,可以含有2個相同的取代基,且處于對位,為![]() ,若含有3個取代基時,取代基不可能相同,苯環上取代至少有2種,故不可能含有3個取代基,可以4個取代基,為2個-Br、2個-CH3,分別為
,若含有3個取代基時,取代基不可能相同,苯環上取代至少有2種,故不可能含有3個取代基,可以4個取代基,為2個-Br、2個-CH3,分別為 、
、 、
、 、
、 、
、 、
、 ,故符合條件的同分異構體共有7種,其中核磁共振氫譜有兩組峰,且峰面積比為1:1的是
,故符合條件的同分異構體共有7種,其中核磁共振氫譜有兩組峰,且峰面積比為1:1的是![]() ,
,
因此,本題正確答案是:7;![]() 。
。


 快樂5加2金卷系列答案
快樂5加2金卷系列答案科目:高中化學 來源: 題型:
【題目】(1)有機物A(![]() )與
)與![]() 溶液反應顯出顏色且苯環上有兩個取代基的同分異構體有___種,試分別寫出其結構簡式:___。
溶液反應顯出顏色且苯環上有兩個取代基的同分異構體有___種,試分別寫出其結構簡式:___。
(2)M的化學式為C4H9Cl,已知A的核磁共振氫譜表明其只有一種氫原子,則M的化學名稱為___。
(3)寫出同時滿足下列條件的分子式為C6H10O4的所有結構簡式:___。
①只含一種官能團②鏈狀結構且無—O—O—③核磁共振氫譜只有2組峰
(4)某化合物B是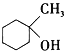 的同分異構體,且分子中只有兩種不同化學環境的氫原子。寫出該化合物的結構簡式:___(任寫一種)。
的同分異構體,且分子中只有兩種不同化學環境的氫原子。寫出該化合物的結構簡式:___(任寫一種)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數的值。下列說法正確的是( )
A.100g30%CH3COOH溶液中含氫原子數為2NA
B.標準狀況下,11.2LCCl4中含有的C—Cl鍵的數目為2NA
C.16gO3和O2混合物中含氧原子數為NA
D.精煉銅過程中陽極質量減少6.4g時,電路中轉移電子數等于0.2NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】pC類似pH,是指極稀溶液中,溶質物質的量濃度的常用對數負值。如某溶液溶質的濃度為1×10-3mol·L-1,則該溶液中溶質的pC=-lg(1×10-3)=3。如圖為H2CO3在加入強酸或強堿溶液后,平衡時溶液中三種成分的pC-pH圖。下列說法不正確的是

A. H2CO3、HCO3-、CO32-不能在同一溶液中大量共存
B. H2CO3電離平衡常數Ka1≈10-6
C. pH=7時,溶液中存在關系c(HCO![]() )>c(H2CO3)>c(CO
)>c(H2CO3)>c(CO![]() )
)
D. pH=9時,溶液中存在關系c(H+)+c(H2CO3)=c(OH-)+c(CO![]() )
)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)實驗室制氨氣的化學方程式為_________________________。
(2)0.1 mol/LNH4Cl溶液中離子濃度由大到小的順序為____________________。
(3)已知0.5mol的液態甲醇(CH3OH)在空氣中完全燃燒生成CO2氣體和液態水時放出350kJ的熱量,則表示甲醇燃燒熱的熱化學方程式為______________________。
(4)已知①C(s)+O2(g)= CO2(g) ΔH1=-393 kJ/mol
②2CO(g)+O2(g)= 2CO2(g) ΔH2=-566 kJ/mol
③TiO2(s)+2Cl2(g)= TiCl4(s)+O2(g) ΔH3=+141 kJ/mol
則TiO2(s)+2Cl2(g)+2C(s)= TiCl4(s)+2CO(g)的 ΔH =__________________。
(5)在25℃下,向濃度均為0.1 mol/L的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成沉淀_____(填化學式)(已知25℃時Ksp[Mg(OH)2]=1.8×10-11,KsP[Cu(OH)2]=2.2×10-20)。
(6)常溫下,0.lmol/LNaHCO3溶液的pH大于8,則溶液中c(H2CO3)______c(CO32-)(填“>”、“=”或“<”)。
(7)在25℃下,將a mol/L的氨水與0.01 mol/L的鹽酸等體積混合,反應完成后溶液中c(NH4+)=c(Cl-),則溶液顯_________性(填“酸”“堿”或“中”),a _________0.01 mol/L(填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,下列各組粒子在指定溶液中能大量共存的是
A.含大量Fe3+的溶液中:NH4+、Mg2+、Cl-、HS-
B.加入Al有H2生成的溶液中Cu2+、NH4+、Cl-、NO3-
C.使酚酞變紅的溶液中:K+、Na+、AlO2-、CO32-
D.小蘇打溶液中:K+、Al3+、Cl-、SO42-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鈉離子電池具有成本低、能量轉換效率高、壽命長等優點。一種鈉離子電池用碳基材料(NamCn)作負極,利用鈉離子在正負極之間嵌脫過程實現充放電,該鈉離子電池的工作原理為:![]()
![]()
![]() 。下列說法不正確的是( )
。下列說法不正確的是( )
A. 充電時,陰極質量減小且Na+數目增加
B. 充電時,陽極的電極反應式為NaCoO2-me-=Na1-mCoO2+mNa+
C. 放電時,Na+向正極移動
D. 放電時,負極的電極反應式為NamCn-me-=mNa++Cn
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某新型電池材料結構如圖,M、W、X、Y、Z是同周期主族元素,除M外均滿足8電子穩定結構,X的最外層電子數是W次外層電子數的3倍,下列說法正確的是
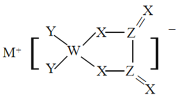
A.M的單質可以保存在煤油中
B.原子半徑Z>X>Y
C.氣態氫化物穩定性X>Y
D.W的最高價氧化物對應的水化物為三元弱酸
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com