
【題目】對人體健康不會造成危害的事實是
A. 用工業酒精(含甲醇)兌制飲用白酒 B. 用福爾馬林浸泡海產品進行防腐保鮮
C. 用二氧化硫漂白食物 D. 在食用鹽中加入碘酸鉀以消除碘缺乏病
 名師伴你成長課時同步學練測系列答案
名師伴你成長課時同步學練測系列答案科目:高中化學 來源: 題型:
【題目】室溫下,1mol·L-l的某二元酸H2A溶液中,存在的HA-、A2-的物質的量分數隨pH變化的關系如圖所示,
下列說法不正確的是
A. H2A的電離方程式為:H2A==H++HA- HA-![]() A2-+H+
A2-+H+
B. 室溫下,電離平衡HA-![]() A2-+H+的平衡常數Ka=10-3。
A2-+H+的平衡常數Ka=10-3。
C. 等物質的量濃度NaHA和Na2A溶液等體積混合,離子濃度大小關系為:c(Na+)>c(HA-)>c(A2-)
D. 在Na2A溶液中存在c(Na+)=2c(A2-)+2c(HA-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯氣是一種重要的化工原料,在生活和生產中的應用十分廣泛。
請回答:
(1)在工業上,“氯堿工業”是生產氯氣的主要方法。請寫出工業制備氯氣的離子方程式__________________________。
(2)實驗室常用MnO2 與濃鹽酸反應制備Cl2,裝置如圖1所示:
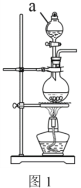
儀器a的名稱為______。制備實驗開始時,先檢査裝置氣密性,接下來的操作依次是:___________(填序號)。
①往燒瓶中加入MnO2粉末 ②加熱 ③往燒瓶中加入濃鹽酸
(3)為證明Cl2與H2O反應為可逆反應,將生成的氣體通入圖2所示裝置:

①裝置A中應加入的試劑是____________。
②證明可逆反應,需驗證在B中反應物和生成物同時存在,證明氯水中有Cl2存在的現象是______,僅使用一種試劑證明氯水中HCl和HClO均存在,合適的試劑是_____。
A.AgNO3溶液 B.石蕊試液
C.NaOH溶液 D.品紅溶液
③裝置C中NaOH溶液的作用是___________________。
(4)制備反應會因鹽酸濃度下降而停止,為測定反應殘余液中鹽酸的濃度(殘余液體積已知)。甲同學提出下列具體方案。請你從下列實驗方案中選擇合理的實驗方法______。
A.在殘余液中加入足量AgNO3溶液,過濾,洗滌,干燥,稱量沉淀的質量
B.在殘余液中加入足量NaHCO3固體,將反應后的氣體直接用堿石灰吸收,測定生成的氣體的質量
C.在殘余液中加入足量鋅片,測量生成氣體的體積,折算成標準狀況下的體積
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】【化學—選修5有機化合物】甲苯是有機化工生產的基本原料之一。利用乙醇和甲苯為原料,可按下列路線合成分子式均為C9H10O2的有機化工產品E和J。

已知:
請回答:
(1)寫出下列反應方程式
①B+D→E______________________________________。
②G→H________________________________________。
(2)①的反應類型為__________;②的反應類型為__________;F的結構簡式為__________。
(3)E、J有多種同分異構體,寫出符合下列條件的4種同分異構體的結構簡式。要求:①與E、J屬同類物質②苯環上有兩個取代基且苯環上的一氯代物只有兩種。
__________________________________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)如果 是某單烯烴與氫氣加成后的產物,則此烯烴可能有_____________種結構;如果是炔烴與氫氣加成的產物,則此炔烴可能有_____________種結構。
是某單烯烴與氫氣加成后的產物,則此烯烴可能有_____________種結構;如果是炔烴與氫氣加成的產物,則此炔烴可能有_____________種結構。
(2)已知某有機物的結構簡式為:
①該有機物發生加成聚合反應(加聚反應)后,所得產物的結構簡式為_____________。
②寫出該有機物與Cl2發生加成反應的化學方程式(注明反應條件):_____________________。
③寫出該有機物在NaOH和醇溶液作用下發生消去反應的化學方程式(注明反應條件):_________________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關說法正確的是
A. 鉛蓄電池放電時的負極和正極的質量均增加
B. MgO(s)+C(s)![]() Mg(s)+CO(g)在室溫下不能自發進行,說明該反應的△H <0
Mg(s)+CO(g)在室溫下不能自發進行,說明該反應的△H <0
C. 對于發應2H2O2![]() 2H2O+O2↑,加入MnO2或升高溫度都能加快O2的生成速率
2H2O+O2↑,加入MnO2或升高溫度都能加快O2的生成速率
D. H2O與金屬Na反應生成1molH2,反應中轉移的電子數為6.02×1023
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表為元素周期表的一部分,a、b、c……為部分元素。回答下列問題:

(1)請寫出上述元素c原子基態核外電子排布式_______________; d+基態核外電子排布式_______________________________。
(2)請寫出一個能比較f、h非金屬性強弱的反應的化學方程式___________________。
(3)請比較f、h、i 三種元素的第一電離能由大到小的順序________(寫元素符號);b、e、j三種元素的電負性由大到小的順序________(寫元素符號)。i2-與b+兩種微粒半徑大小: i2-___b+ (填>、=或<)。
(4)請寫出e 元素最高價氧化物對應的水化物與a、b、i三種元素形成的化合物反應 的離子方程式___________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學利用下列裝置探究Na與CO2反應的還原產物,已知PdCl2+CO+H2O==Pd(黑色)↓+CO2+2HCl。下列相關分析錯誤的是
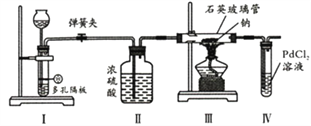
A. I中發生反應可以是Na2CO3+H2SO4==Na2SO4+H2O+CO2↑
B. II中濃硫酸的目的是干燥CO2
C. 實驗時,III中石英玻璃管容易受到腐蝕
D. 步驟IV的目的是證明還原產物是否有CO
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com