
【題目】(1)X射線衍射測(cè)定等發(fā)現(xiàn),I3AsF6中存在I3+離子。I3+離子的幾何構(gòu)型為_____,中心原子的雜化類型為_____。
(2)CS2分子中,C原子的雜化軌道類型是_____。
(3)F2通入稀NaOH溶液中可生成OF2,OF2分子構(gòu)型為_____,其中氧原子的雜化方式為_____。
(4)CH3COOH中C原子軌道雜化類型為_____。
【答案】V形 sp3 sp V形 sp3 sp3、sp
【解析】
根據(jù)價(jià)層電子對(duì)互拆理論分析中心原子的價(jià)層電子對(duì)數(shù),并確定其雜化類型和分子的空間構(gòu)型。
(1)X射線衍射測(cè)定等發(fā)現(xiàn),I3AsF6中存在I3+離子。I3+離子的價(jià)層電子對(duì)數(shù)為![]() ,由于中心原子只形成2個(gè)共價(jià)鍵,故其有2個(gè)孤電子對(duì),故其幾何構(gòu)型為V形,中心原子的雜化類型為sp3。
,由于中心原子只形成2個(gè)共價(jià)鍵,故其有2個(gè)孤電子對(duì),故其幾何構(gòu)型為V形,中心原子的雜化類型為sp3。
(2)CS2分子中,C原子價(jià)層電子對(duì)數(shù)為![]() ,中心原子沒(méi)有孤電子對(duì),故其雜化軌道類型是sp。
,中心原子沒(méi)有孤電子對(duì),故其雜化軌道類型是sp。
(3)OF2分子的中心原子的價(jià)層電子對(duì)數(shù)為![]() ,中心原子還有2個(gè)孤電子對(duì),故其分子的空間構(gòu)型為V形,其中氧原子的雜化方式為sp3。
,中心原子還有2個(gè)孤電子對(duì),故其分子的空間構(gòu)型為V形,其中氧原子的雜化方式為sp3。
(4)CH3COOH中C原子有兩種,甲基中的碳原子與相鄰原子形成4個(gè)共用電子對(duì)、沒(méi)有孤電子對(duì),故其軌道雜化類型為sp3;羧基中的碳原子與氧原子形成雙鍵,還分別與甲基上的碳原子、羥基中的氧原子各形成1個(gè)共用電子對(duì),沒(méi)有孤電子對(duì),故其軌道雜化類型為sp2。


 閱讀快車系列答案
閱讀快車系列答案
| 年級(jí) | 高中課程 | 年級(jí) | 初中課程 |
| 高一 | 高一免費(fèi)課程推薦! | 初一 | 初一免費(fèi)課程推薦! |
| 高二 | 高二免費(fèi)課程推薦! | 初二 | 初二免費(fèi)課程推薦! |
| 高三 | 高三免費(fèi)課程推薦! | 初三 | 初三免費(fèi)課程推薦! |
科目:高中化學(xué) 來(lái)源: 題型:
【題目】在一密閉容器中加入A、B、C三種氣體,保持一定溫度,在t1~t4時(shí)刻測(cè)得各物質(zhì)的濃度如下表。據(jù)此判斷下列結(jié)論正確的是( )
測(cè)定時(shí)刻/s | t1 | t2 | t3 | t4 |
c(A)/(mol/L) | 6 | 3 | 2 | 2 |
c(B)/(mol/L) | 5 | 3.5 | 3 | 3 |
c(C)/(mol/L) | 1 | 2.5 | 3 | 3 |
A.在t3時(shí)刻反應(yīng)已經(jīng)停止
B.A的轉(zhuǎn)化率比B的轉(zhuǎn)化率低
C.在容器中發(fā)生的反應(yīng)為:2A+B![]() 2C
2C
D.在t2~t3內(nèi)A的平均反應(yīng)速率為:[1/(t3-t2)]mol/(L·s)
查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:
【題目】為了強(qiáng)化安全管理,某油庫(kù)引進(jìn)一臺(tái)測(cè)空氣中汽油含量的測(cè)量?jī)x,其工作原理如圖所示(用強(qiáng)酸性溶液作電解質(zhì)溶液)。下列說(shuō)法不正確的是
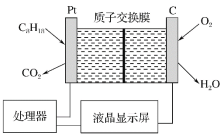
A.石墨電極作正極,發(fā)生還原反應(yīng)
B.鉑電極的電極反應(yīng)式:C8H18+16H2O-50e-===8CO2↑+50H+
C.H+由質(zhì)子交換膜左側(cè)向右側(cè)遷移
D.每消耗 5.6 L O2,電路中通過(guò) 1 mol 電子
查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:
【題目】下列說(shuō)法錯(cuò)誤的是( )
A. 在NH![]() 和[Cu(NH3)4]2+中都存在配位鍵
和[Cu(NH3)4]2+中都存在配位鍵
B. H2O是極性分子,分子中O原子不處在2個(gè)H原子所連成的直線的中央
C. SO2、SO3、BF3、NCl3都是極性分子
D. 向含有0.1 mol [Co(NH3)4Cl2]Cl的水溶液中加入足量AgNO3溶液只能生成0.1 mol AgCl
查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:
【題目】寫(xiě)出下列有機(jī)物的類別及所含官能團(tuán)的名稱。
(1)CH3CH=CH2____、_________;
(2)HC≡C—CH2CH3__________、__________;
(3)![]() _________、___________;
_________、___________;
(4)![]() _________、_________;
_________、_________;
(5)![]() _________、___________;
_________、___________;
(6)CH3CH2—O—CH3__________、__________。
查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:
【題目】前四周期元素A、B、C、D、E、F的原子序數(shù)依次增大。A原子的陰離子的電子排布式與基態(tài)鋰離子的相同,A和E位于同主族,基態(tài)B原子核外有3個(gè)能級(jí)且各能級(jí)上容納的電子數(shù)相等,基態(tài)D原子有2個(gè)未成對(duì)電子,最外能層符號(hào)為L。+1價(jià)F離子的3d能級(jí)達(dá)到全充滿結(jié)構(gòu)。
回答下列問(wèn)題:
(1)基態(tài)C原子價(jià)電子排布圖為_____。
(2)B、C、D三種元素第一電離能由大到小排序?yàn)?/span>_____(填元素符號(hào),下同),它們的電負(fù)性由小到大排序?yàn)?/span>_____。
(3)C、F組成的晶體的晶胞如圖1所示。已知該晶體密度為ρg·cm-3,NA代表阿伏加德羅常數(shù),則C、F最近的核間距為_____cm。
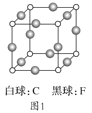
(4)A和E組成晶體,其晶胞如圖2所示。E粒子周圍有_____個(gè)E緊密相鄰且最近;連接與E等距離且最近的A粒子構(gòu)成的形狀是_____。

查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:
【題目】下列說(shuō)法錯(cuò)誤的是
A. 0.1mol/L的Na2CO3溶液加適量水稀釋后,溶液中![]() 變大
變大
B. 若使Na2S溶液中![]() 接近于2︰1,可加入適量的KOH固體
接近于2︰1,可加入適量的KOH固體
C. 25℃時(shí),濃度均為0. 1mol/L NaOH和NH3·H2O混合溶液中c(OH- )>c(Na+ )=c(NH3·H2O)
D. 0.2 mol/L CH3COOH溶液與0. 1mol/L NaOH溶液等體積混合:2c(H+)-2c(OH -)=c(CH3COO-)-c(CH3COOH)
查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:
【題目】除了酸以外,某些鹽也能溶解沉淀。利用如表三種試劑進(jìn)行實(shí)驗(yàn),相關(guān)分析不正確的是
編號(hào) | ① | ② | ③ |
分散質(zhì) | Mg(OH)2 | HCl | NH4Cl |
備注 | 懸濁液 | 1mol/L | 1mol/L |
A.向①中加入②,c(OH-)減小,Mg(OH)2溶解平衡正向移動(dòng)
B.向①中加入酚酞顯紅色說(shuō)明物質(zhì)的“不溶性”是相對(duì)的
C.向①中加入③沉淀溶解,說(shuō)明Mg(OH)2比NH3·H2O更難電離
D.①、③混合后發(fā)生反應(yīng):Mg(OH)2(s)+2NH4+![]() Mg2++2NH3·H2O
Mg2++2NH3·H2O
查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:
【題目】25℃時(shí),向一定濃度的Na2C2O4溶液中滴加鹽酸,混合溶液的pH與離子濃度變化關(guān)系如圖所示。已知H2C2O4是二元弱酸,X表示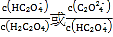 ,下列敘述錯(cuò)誤的是
,下列敘述錯(cuò)誤的是
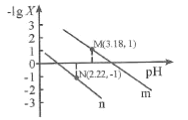
A.從M點(diǎn)到N點(diǎn)的過(guò)程中,c(H2C2O4)逐漸增大
B.直線n表示pH與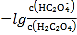 的關(guān)系
的關(guān)系
C.由N點(diǎn)可知Ka1 (H2C2O4)的數(shù)量級(jí)為10 -2
D.pH=4.18的混合溶液中:c(Na+)>c(HC2O4-)= c(C2O42-) =c(Cl-)> c(H+)>c(OH-)
查看答案和解析>>
國(guó)際學(xué)校優(yōu)選 - 練習(xí)冊(cè)列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺(tái) | 網(wǎng)上有害信息舉報(bào)專區(qū) | 電信詐騙舉報(bào)專區(qū) | 涉歷史虛無(wú)主義有害信息舉報(bào)專區(qū) | 涉企侵權(quán)舉報(bào)專區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com