【答案】
分析:Ⅰ(1)化學平衡常數,是指在一定溫度下,可逆反應達到平衡時各生成物濃度的化學計量數次冪的乘積除以各反應物濃度的化學計量數次冪的乘積所得的比值,據此書寫;
該反應正反應是放熱反應,升高溫度平衡向逆反應方向移動,據此判斷溫度對平衡常數的影響;
(2)根據v=
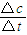
計算v(NH
3),再根據速率之比等于化學計量數之比計算v(H
2);
(3)若平衡時,移走1mol N
2和3mol H
2,等效為原平衡體積增大一倍,降低壓強,若平衡不移動,則c(NH
3)=0.25mol/L,但平衡向逆反應移動;
Ⅱ(1)0.4mol/LCH
3COOH溶液和0.2mol/LNaOH溶液各100mL混合,反應后的溶液中含CH
3COOH、CH
3COONa各0.02mol,溶液pH=5,說明醋酸的電離程度大于醋酸根的水解程度,據此判斷排序;
(2)①根據物料守恒計算;
②根據物料守恒、電荷守恒計算;
Ⅲ.根據Ksp[Fe(OH)
3]=c(Fe
3+)?c
3(OH
-),Kw=c(H
+)?c(OH
-)及Fe(OH)
3+3H
+?Fe
3++3H
2O的平衡常數表達式,可得3個常數的關系,進行計算.
根據Ksp[Fe(OH)
3]=c(Fe
3+)?c
3(OH
-)計算c(OH
-),再根據Kw=c(H
+)?c(OH
-)計算c(H
+),最后根據pH=-lgc(H
+)計算.
解答:解:Ⅰ(1)N
2(g)+3H
2(g)?2NH
3(g)平衡常數k=
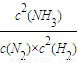
,該反應正反應是放熱反應,升高溫度平衡向逆反應方向移動,平衡常數變小,
故答案為:

;變小;
(2)5min后達到平衡,測得c(NH
3)=0.5mol/L,則v(NH
3)=
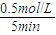
=0.1mol/(L?min),速率之比等于化學計量數之比,v(H
2)=1.5v(NH
3)=1.5×0.1mol/(L?min)=0.15mol/(L?min);
故答案為:0.15mol/(L?min);
(3)若平衡時,移走1mol N
2和3mol H
2,等效為原平衡體積增大一倍,降低壓強,若平衡不移動,則c(NH
3)=0.25mol/L,但平衡向逆反應移動,故平衡時c(NH
3)<0.25mol/L,
故答案為:<;
Ⅱ(1)0.4mol/LCH
3COOH溶液和0.2mol/LNaOH溶液各100mL混合,反應后的溶液中含CH
3COOH、CH
3COONa各0.02mol,溶液pH=5,溶液呈酸性,則c(H
+)>c(OH-),說明醋酸的電離程度大于醋酸根的水解程度,則c(CH
3COO
-)>c(Na
+),醋酸是弱電解質,不能完全電離,則c(Na
+)>c(H
+),故離子濃度由大到小的順序是:c(CH
3COO
-)>c(Na
+)>c(H
+)>c(OH
-),
故答案為:c(CH
3COO
-)>c(Na
+)>c(H
+)>c(OH
-);
(2)①反應后的溶液中含CH
3COOH、CH
3COONa各0.02mol,溶液體積為200mL,根據物料守恒可知,c(CH
3COO
-)+c(CH
3COOH)=

=0.2moL/L,
故答案為:0.2;
②根據物料守恒有:c(CH
3COO
-)+c(CH
3COOH)=2c(Na
+),
根據電荷守恒有:c(Na
+)+c(H
+)=c(OH
-)+c(CH
3COO
-),
整理得:c(CH
3COO
-)+c(CH
3COOH)=2[c(OH
-)+c(CH
3COO
-)-c(H
+)]
即c(CH
3COO
-)-c(CH
3COOH)=2[c(H
+)-c(OH
-)]=2×(10
-5-10
-9)mol/L
故答案為:2×(10
-5-10
-9);
8Ⅲ.Fe(OH)
3+3H
+?Fe
3++3H
2O的平衡常數表達式k=
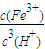
,由Ksp[Fe(OH)
3]=c(Fe
3+)?c
3(OH
-),Kw=c(H
+)?c(OH
-),可知式k=
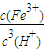
=
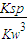
=
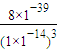
=8×10
3,
向0.001mob/L FeCl
3溶液中通入氨氣(體積變化忽略不計),開始沉淀時溶液中c(OH
-)=
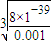
=2×10
-12mol/L,故c(H
+)=
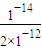
=5×10
-3mol/L,故pH=-lgc(H
+)=-lg5×10
-3=2.3,
故答案為:8×10
3;2.3.
點評:本題屬于拼合型題目,涉及化學平衡與反應速率、鹽類水解、平衡常數的有關計算等,題目綜合性較大,難度中等,是一道不錯的能力考查題,注意基礎知識的理解掌握.

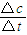 計算v(NH3),再根據速率之比等于化學計量數之比計算v(H2);
計算v(NH3),再根據速率之比等于化學計量數之比計算v(H2);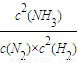 ,該反應正反應是放熱反應,升高溫度平衡向逆反應方向移動,平衡常數變小,
,該反應正反應是放熱反應,升高溫度平衡向逆反應方向移動,平衡常數變小, ;變小;
;變小;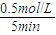 =0.1mol/(L?min),速率之比等于化學計量數之比,v(H2)=1.5v(NH3)=1.5×0.1mol/(L?min)=0.15mol/(L?min);
=0.1mol/(L?min),速率之比等于化學計量數之比,v(H2)=1.5v(NH3)=1.5×0.1mol/(L?min)=0.15mol/(L?min); =0.2moL/L,
=0.2moL/L,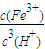 ,由Ksp[Fe(OH)3]=c(Fe3+)?c3(OH-),Kw=c(H+)?c(OH-),可知式k=
,由Ksp[Fe(OH)3]=c(Fe3+)?c3(OH-),Kw=c(H+)?c(OH-),可知式k=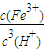 =
=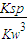 =
=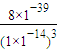 =8×103,
=8×103,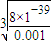 =2×10-12mol/L,故c(H+)=
=2×10-12mol/L,故c(H+)=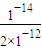 =5×10-3mol/L,故pH=-lgc(H+)=-lg5×10-3=2.3,
=5×10-3mol/L,故pH=-lgc(H+)=-lg5×10-3=2.3,


 .
.
 能源短缺是人類面臨的重大問題.甲醇是一種可再生能源,具有廣泛的開發和應用前景.
能源短缺是人類面臨的重大問題.甲醇是一種可再生能源,具有廣泛的開發和應用前景.