
【題目】1 mol某有機物在稀硫酸作用下,水解生成2 mol相同的物質。有下列物質:
①蔗糖 ②麥芽糖 ③淀粉 ④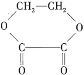 ⑤
⑤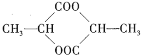
⑥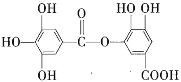 ⑦
⑦![]()
其中符合此題目要求的是( )
A.②⑤⑥⑦B.②④⑤⑦C.①②⑤⑦D.①④⑤⑥
 星級口算天天練系列答案
星級口算天天練系列答案 芒果教輔達標測試卷系列答案
芒果教輔達標測試卷系列答案科目:高中化學 來源: 題型:
【題目】相同溫度、相同容積的四個密閉容器中進行同樣的可逆反應:2X(g)+Y(g)![]() 3W(g)+2Z(g) △H=﹣Q KJ/mol,起始時充入氣體的物質的量及平衡時體系能量變化數(shù)據(jù)如表,下列說法正確的是( )
3W(g)+2Z(g) △H=﹣Q KJ/mol,起始時充入氣體的物質的量及平衡時體系能量變化數(shù)據(jù)如表,下列說法正確的是( )
X | Y | W | Z | 反應體系能量變化 | |
甲 | 2mol | 1mol | 放出a kJ/mol | ||
乙 | 1mol | 1mol | 放出b kJ/mol | ||
丙 | 2mol | 2mol | 放出c kJ/mol | ||
丁 | 3mol | 2mol | 吸收d kJ/mol |
A.X的轉化率為:甲<乙<丙
B.c+d<Q
C.平衡時,甲容器中的反應速率比丁容器中的慢
D.平衡時丙容器中Z的物質的量濃度最大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】
鉀和碘的相關化合物在化工、醫(yī)藥、材料等領域有著廣泛的應用。回答下列問題:
(1)元素K的焰色反應呈紫紅色,其中紫色對應的輻射波長為_______nm(填標號)。
A.404.4 B.553.5 C.589.2 D.670.8 E.766.5
(2)基態(tài)K原子中,核外電子占據(jù)的最高能層的符號是_________,占據(jù)該能層電子的電子云輪廓圖形狀為___________。K和Cr屬于同一周期,且核外最外層電子構型相同,但金屬K的熔點、沸點等都比金屬Cr低,原因是___________________________。
(3)X射線衍射測定等發(fā)現(xiàn),I3AsF6中存在I3+離子。I3+離子的幾何構型為_____________,中心原子的雜化形式為________________。
(4)KIO3晶體是一種性能良好的非線性光學材料,具有鈣鈦礦型的立體結構,邊長為a=0.446nm,晶胞中K、I、O分別處于頂角、體心、面心位置,如圖所示。K與O間的最短距離為______nm,與K緊鄰的O個數(shù)為__________。
(5)在KIO3晶胞結構的另一種表示中,I處于各頂角位置,則K處于______位置,O處于______位置。
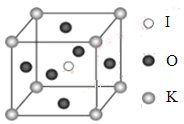
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】配位鍵是一種特殊的化學鍵,其中共用電子對由某原子單方面提供。如![]() 就是由
就是由![]() (氮原子提供共用電子對)和
(氮原子提供共用電子對)和![]() (缺電子)通過配位鍵形成的。據(jù)此回答下列問題。
(缺電子)通過配位鍵形成的。據(jù)此回答下列問題。
(1)下列粒子中存在配位鍵的是__________(填序號)
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
(2)硼酸(![]() )溶液呈酸性,試寫出其電離方程式:____________________。
)溶液呈酸性,試寫出其電離方程式:____________________。
(3)科學家對![]() 結構的認識經歷了較為漫長的過程,最初科學家提出了兩種觀點:
結構的認識經歷了較為漫長的過程,最初科學家提出了兩種觀點:
甲: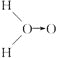 (式中O→O表示配位鍵,在化學反應中O→O鍵遇到還原劑時易斷裂)
(式中O→O表示配位鍵,在化學反應中O→O鍵遇到還原劑時易斷裂)
乙:HOOH
化學家Baeyer和Villiyer為研究H2O2的結構,設計并完成了下列實驗:
a.將C2H5OH與濃H2SO4反應生成(C2H5)2SO4和水;
b.將制得的(C2H5)2SO4與H2O2反應,只生成A和H2SO4;
c.將生成的A與H2反應(已知該反應中H2作還原劑)。
①如果H2O2的結構如甲所示,實驗c中化學反應方程式為(A寫結構簡式)________________。
②為了進一步確定H2O2的結構,還需要在實驗c后添加一步實驗d,請設計d的實驗方案:____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】臭氧(![]() )能吸收紫外線,保護人類賴以生存的環(huán)境。
)能吸收紫外線,保護人類賴以生存的環(huán)境。![]() 分子的結構如圖所示,呈
分子的結構如圖所示,呈![]() 形,鍵角為
形,鍵角為![]() ,中間的一個氧原子與另外兩個氧原子分別構成一個非極性共價鍵。中間氧原子提供2個電子,旁邊兩個氧原子各提供一個電子,構成一個特殊的化學鍵大
,中間的一個氧原子與另外兩個氧原子分別構成一個非極性共價鍵。中間氧原子提供2個電子,旁邊兩個氧原子各提供一個電子,構成一個特殊的化學鍵大![]() 鍵(虛線內部分),分子中三個氧原子共用這4個電子。請回答:
鍵(虛線內部分),分子中三個氧原子共用這4個電子。請回答:
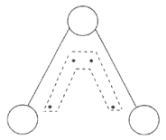
(1)![]() 中的非極性共價鍵是__________鍵。
中的非極性共價鍵是__________鍵。
(2)分子中的大![]() 鍵可用符號
鍵可用符號![]() 表示,其中m代表參與形成大
表示,其中m代表參與形成大![]() 鍵的原子數(shù),n代表參與形成大
鍵的原子數(shù),n代表參與形成大![]() 鍵的電子數(shù)(如苯分子中的大
鍵的電子數(shù)(如苯分子中的大![]() 鍵可表示為
鍵可表示為![]() ),則
),則![]() 中的大
中的大![]() 鍵應表示為__________。
鍵應表示為__________。
(3)臭氧與氧氣的關系是__________。
(4)下列物質的分子與![]() 分子的結構最相似的是__________(填序號)。
分子的結構最相似的是__________(填序號)。
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】由人體尿液分離出來的結晶化合物A,熔點為187~188℃。現(xiàn)對化合物A進行如下實驗:
(1)A的蒸氣密度為8.0 g/L (已折合成標準狀況)。取17.90 g A完全燃燒,將生成的氣體先通過濃硫酸,濃硫酸質量增加8.10 g,再將剩余氣體通過堿石灰,氣體質量減輕39.60 g;另取17.90 g A使其完全分解,可得到1.12 L (標準狀況)氮氣。則A的分子式為_________________。
(2)A和足量6 mol/L的鹽酸混合加熱可以完全水解,1 mol A水解可生成1 mol B和1 mol C。已知:A、B、C三種物質的分子中均含有一個羧基;B僅由碳、氫、氧三種元素組成,三種元素原子的物質的量之比為7∶6∶2;C的名稱為甘氨酸。試寫出A的結構簡式:_____________,B的分子式:_________,C的一種同分異構體的結構簡式:_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】溫度為T1時,在三個容積均為1 L的恒容密閉容器中僅發(fā)生反應 2NO2(g)2NO(g)+O2(g) ΔH>0。實驗測得:υ正=υ(NO2)消耗=k正c2(NO2),υ逆=υ(NO)消耗=2υ(O2)消耗=k逆c2(NO)·c(O2),k正、k逆為速率常數(shù),受溫度影響。下列說法正確的是( )
容器編號 | 物質的起始濃度(mol·L-1) | 物質的平衡濃度(mol·L-1) | ||
c(NO2) | c(NO) | c(O2) | c(O2) | |
Ⅰ | 0.6 | 0 | 0 | 0.2 |
Ⅱ | 0.3 | 0.5 | 0.2 | |
Ⅲ | 0 | 0.5 | 0.35 | |
A.反應達平衡時,容器Ⅰ與容器Ⅱ中的總壓強之比為1∶1
B.反應達平衡時,容器Ⅱ中![]() 比容器Ⅰ中的大
比容器Ⅰ中的大
C.反應達平衡時,容器Ⅲ中NO的體積分數(shù)大于50%
D.當溫度改變?yōu)?/span>T2時,若k正=k逆,則T2>T1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在容積為1 L的容器中,通入一定量的N2O4,發(fā)生反應N2O4(g)![]() 2NO2(g),隨溫度升高,混合氣體的顏色變深。回答下列問題:
2NO2(g),隨溫度升高,混合氣體的顏色變深。回答下列問題:
(1)反應的ΔH_____0(填“大于”或“小于”);100 ℃時,體系中各物質濃度隨時間變化如圖所示。在 0~60 s 時段, 反應速率 v(N2O4)為_____mol·L-1·s-1;反應的平衡轉化率為:_____; 反應的平衡常數(shù)K1為_____。
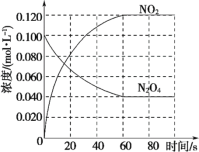
(2)100℃時達平衡后,改變反應溫度為 T,N2O4以0.002 0 mol·L-1·s-1的平均速率降低,經10 s又達到平衡。
a:T____________100℃(填“大于”或“小于”),判斷理由是__________。
b:計算溫度T時反應的平衡常數(shù)K2____________。
(3)溫度T時反應達平衡后,將反應容器的容積減少一半。平衡向____________(填“正反應”或“逆反應”)方向移動,判斷理由________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】輝鉬精礦主要成分是二氧化鉬(MoS2),還含有石灰石、石英、黃銅礦(CuFeS2)等雜質。某學習小組設計提取MoS2的過程如下:下列說法錯誤的是
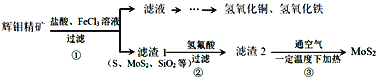
A.為加快輝鉬精礦溶解,可將礦石粉粹并適當加熱
B.加濾液中含Ca2+、Fe2+、Fe3+、Cu2+、H+等離子
C.以上①②③過程均涉及氧化還原反應
D.步驟③溫度不宜過高,以免MoS2被氧化
查看答案和解析>>
國際學校優(yōu)選 - 練習冊列表 - 試題列表
湖北省互聯(lián)網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com