
【題目】實驗室可用NaBr、濃硫酸、乙醇等為原料制備少量溴乙烷(反應裝置如圖所示):C2H5—OH+HBr![]() C2H5—Br+H2O
C2H5—Br+H2O
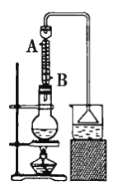
已知物質的用量:0.30molNaBr(s);0.25mol乙醇(密度為0.80g·cm-3);36mL濃硫酸(質量分數為98%,密度為1.84g·mL-1);25mL水。試回答下列問題:
(1)反應裝置中燒瓶的容積應選擇__(填序號)。
A.50mL B.100mL C.150mL D.250mL
(2)冷凝管中的冷凝水的流向應是__(填序號)。
A.A進B出 B.B進A出 C.從A進或B進均可
(3)實驗完成后,需將燒瓶內的有機物蒸出,結果得到棕黃色的粗溴乙烷,欲得純凈的溴乙烷,應采取的操作是___。
(4)某同學在溴乙烷中加入NaOH乙醇溶液并加熱,為判斷其發生的是水解反應還是消去反應,則該同學向反應后的溶液中應加入的試劑是__。
【答案】C B 將粗溴乙烷和稀![]() 溶液的混合物放在分液漏斗中用力振蕩,并不斷放氣,至油層無色,分液可得純溴乙烷 稀鹽酸、溴水
溶液的混合物放在分液漏斗中用力振蕩,并不斷放氣,至油層無色,分液可得純溴乙烷 稀鹽酸、溴水
【解析】
(1)燒瓶內所盛液體的體積不應超過其容積的三分之二,但也不能少于容積的四分之一,計算液體的體積和,便可確定所選燒瓶的規格。
(2)冷凝管中的冷凝水流向應是下進上出。
(3)溴乙烷中常會混有溴而使其顯棕黃色,應加入堿溶液處理。
(4)水解反應主產物為乙醇,消去反應主產物為乙烯,選擇能區分二者的試劑,便可確定發生反應的類型。
(1)乙醇的體積為![]() =14.4mL,濃硫酸的體積為36mL,水的體積為25mL,液體的總體積為75.3mL,按“燒瓶內所盛液體的體積不應超過其容積的三分之二”計算,燒瓶的容積為113mL,故選C。答案為C;
=14.4mL,濃硫酸的體積為36mL,水的體積為25mL,液體的總體積為75.3mL,按“燒瓶內所盛液體的體積不應超過其容積的三分之二”計算,燒瓶的容積為113mL,故選C。答案為C;
(2)為了使冷凝效果更佳,冷凝管中的冷凝水的流向應是下進上出,故選B。答案為B;
(3)除去溴乙烷中的溴,可使用NaOH溶液進行處理,具體操作是將粗溴乙烷和稀![]() 溶液的混合物放在分液漏斗中用力振蕩,并不斷放氣,至油層無色,分液可得純溴乙烷。答案為:將粗溴乙烷和稀
溶液的混合物放在分液漏斗中用力振蕩,并不斷放氣,至油層無色,分液可得純溴乙烷。答案為:將粗溴乙烷和稀![]() 溶液的混合物放在分液漏斗中用力振蕩,并不斷放氣,至油層無色,分液可得純溴乙烷;
溶液的混合物放在分液漏斗中用力振蕩,并不斷放氣,至油層無色,分液可得純溴乙烷;
(4)某同學在溴乙烷中加入NaOH乙醇溶液并加熱,判斷發生的是水解反應還是消去反應,需檢驗產物是乙醇還是乙烯。為方便起見,可檢驗乙烯,從而確定用溴水,但同時需去除NaOH,以防與溴發生反應,所以應加入的試劑是稀鹽酸、溴水。答案為:稀鹽酸、溴水。


科目:高中化學 來源: 題型:
【題目】根據下列圖示所得出的結論不正確的是

A. 圖甲是CO(g)+H2O(g)![]() CO2(g)+H2(g)的平衡常數與反應溫度的關系曲線,說明該反應的ΔH<0
CO2(g)+H2(g)的平衡常數與反應溫度的關系曲線,說明該反應的ΔH<0
B. 圖乙是室溫下H2O2催化分解放出氧氣的反應中c(H2O2 )隨反應時間變化的曲線,說明隨著反應的進行H2O2分解速率逐漸減小
C. 圖丙是室溫下用0.1000 mol·L1NaOH溶液滴定20.00 mL 0.1000 mol·L1某一元酸HX的滴定曲線,說明HX是一元強酸
D. 圖丁是室溫下用Na2SO4除去溶液中Ba2+達到沉淀溶解平衡時,溶液中c(Ba2+ )與c(SO42)的關系曲線,說明溶液中c(SO42 )越大c(Ba2+ )越小
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期主族元素W、X、Y、Z的原子序數依次增大,W在大氣中有兩種同素異形體且均能支持燃燒,X的原子半徑是所有短周期主族元素中最大的,非金屬元素Y的原子序數是Z的最外層電子數的2倍。下列敘述不正確的是( )
A.Y、Z的氫化物穩定性Y>Z
B.Y單質的熔點高于X單質
C.X、W、Z能形成具有強氧化性的XZW
D. 中W和Y都滿足8電子穩定結構
中W和Y都滿足8電子穩定結構
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】1999年1月,俄美科學家聯合小組宣布合成了114號元素的一種同位素原子,其中子數為184,有關該元素和同位素原子的敘述中不正確的是( )
A.該原子位于元素周期表第七周期第![]() 族
族
B.該元素為金屬,性質與![]() 相似
相似
C.該元素相對原子質量是298
D.該元素主要化合價為![]() 和
和![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對傘花烴(a)常用作染料、醫藥、香料的中間體,a可轉化為b(如圖)。下列說法錯誤的是( )

A.常溫下對傘花烴呈液態且難溶于水
B.b物質的一氯代物有5種
C.對傘花烴分子中最多有9個碳原子共平面
D.圖中氫化反應既是加成反應也是還原反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】馬里諾娃博士找到了一種比二氧化碳有效![]() 倍的“超級溫室氣體”全氟丙烷
倍的“超級溫室氣體”全氟丙烷![]() ,并提出用其“溫室化火星”使其成為第二個地球的計劃。有關全氟丙烷的說法正確的是( )
,并提出用其“溫室化火星”使其成為第二個地球的計劃。有關全氟丙烷的說法正確的是( )
A.分子中三個碳原子可能處于同一直線上
B.相同壓強下,沸點:![]()
C.全氟丙烷的電子式為:![]()
D.全氟丙烷中既有極性鍵又有非極性鍵
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述正確的有( )
A.第四周期元素中,錳原子價電子層中未成對電子數最多
B.第二周期主族元素的原子半徑隨核電荷數增大依次減小
C.鹵素氫化物中,![]() 的沸點最低的原因是其分子間的范德華力最小
的沸點最低的原因是其分子間的范德華力最小
D.價層電子對互斥理論中,π鍵電子對數不計入中心原子的價層電子對數
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖是電解飽和 NaCl 溶液的實驗裝置,x、y 都是惰性電極,a 是飽和 NaCl 溶液,同時在兩邊各滴入幾滴酚酞試液,下列有關該實驗正確的說法是

A.x 電極為陽極,y 電極為陰極
B.x 電極附近溶液變紅色,且有刺激性氣味氣體產生
C.若將兩電極產生的氣體收集起來,X電極得到的氣體與Y電極得到的氣體之比之比略大于 1:1
D.電解后,將溶液混勻,電解前后溶液的 pH 未發生變化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是H3AsO4水溶液中含砷的各物種分布分數(平衡時某物種的濃度占各物種濃度之和的分數)與pH的關系。下列說法錯誤的是( )
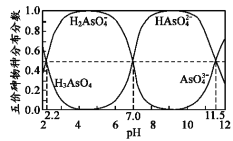
A.NaH2AsO4溶液呈酸性
B.向NaH2AsO4溶液滴加NaOH溶液過程中,c(H2AsO4-)/c(HAsO42-)先增加后減少
C.H3AsO4和HAsO42-在溶液中不能大量共存
D.Ka3(H3AsO4)的數量級為10-12
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com