
【題目】已知常溫下濃度均為0.1mol/L的下列三種溶液的PH:
溶質 | NaHCO3 | Na2CO3 | NaCN |
PH | 9.7 | 11.6 | 11.1 |
下列說法中正確的是
A.溶液中陽離子的物質的量濃度之和:Na 2CO3 >NaCN>NaHCO3
B.相同條件下的酸性:H 2CO3 <HCN
C.三種溶液中均存在電離平衡和水解平衡
D.升高Na 2CO3 溶液的溫度,![]() 減小
減小
 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
【題目】下列關于物質的分離、提純實驗中的一些操作或做法,正確的是
A. 在組裝蒸餾裝置時,溫度計的水銀球應伸入液面下
B. 在苯甲酸重結晶實驗中,粗苯甲酸加熱溶解后還要加少量蒸餾水
C. 用苯萃取溴水時有機層應從下口放出
D. 在苯甲酸重結晶實驗中,待粗苯甲酸完全溶解后,要冷卻到常溫才過濾
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在25℃、1.01×105Pa下,將22gCO2通入到750mL 1.0 mol·L-1的NaOH溶液中充分反應,放出x kJ熱量。在該條件下1molCO2通入到2L 1.0 mol·L-1的NaOH溶液中充分反應,放出ykJ熱量,則CO2與NaOH反應生成NaHCO3的熱化學反應方程式為] ( )
A. CO2(g) + NaOH(aq)=NaHCO3(aq) ΔH=-(2y-x) kJ·mol-1
B. CO2(g) + NaOH(aq)=NaHCO3(aq) ΔH=-(4x-y) kJ·mol-1
C. CO2(g) + NaOH(aq)=NaHCO3(aq) ΔH=-(2x-y) kJ·mol-1
D. CO2(g) + NaOH(aq)=NaHCO3(aq) ΔH=-(8x-2y) kJ·mol-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】pH=1的兩種溶液A、B各1mL,分別加水稀釋到1000mL,分別加水稀釋到1000mL,其pH與溶液體積(V)的關系如圖示,下列說法正確的是
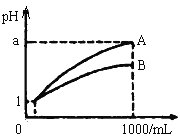
①若a<4,則A、B都是弱酸
②稀釋后,A酸溶液的酸性比B酸溶液強
③若a=4,則A是強酸,B是弱酸
④A、B兩種酸溶液的物質的量濃度一定相等
A.①④ B.②③ C.①③ D.②④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學與生活、生產、環境密切相關,下列有關說法錯誤的是
A. 硒是人體必需的微量元素,但不宜攝入過多
B. 我國最早使用的青銅器主要成分是銅、錫等金屬
C. 用CO2合成可降解的塑料聚碳酸酯,實現“碳”的循環利用
D. 某種驗鈔筆中含有碘酒溶液,遇假鈔呈現藍色,其原理是葡萄糖遇碘變藍
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將10.8g的Ag投入一定量的濃硝酸中完全溶解得到NO和NO2的混合氣體,用NaOH溶液把該混合氣體完全吸收得釗NaNO3和NaNO2的混合溶液,則所得NaNO2的物質的量為
A. 0.05mol B. 0.06mol C. 0.075mol D. 0.1mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】T℃時。體積均為0.5L的兩個恒容密閉容器中發生可逆反應:
2A(g)+B(g)![]() 2C(g)△H=-QkJ/mol(Q>0)
2C(g)△H=-QkJ/mol(Q>0)
實驗測得反應在起始、達到平衡時的有關數據如下表:
容器編號 | 起始時各物質物質的量/mol | 達到平衡時體系能量的變化 | ||
A | B | C | ||
① | 2 | 1 | 0 | 0.75Q kJ |
② | 0.4 | 0.2 | 1.6 | |
下列敘述正確的是
A.容器①、②中反應的平衡常數均為36
B.容器②中反應達到平衡時放出的熱量為0.05 Q kJ
C.向容器①中通入氦氣,平衡時A的轉化率不變
D.其他條件不變,若容器②保持恒容絕熱,則達到平衡時C的體積分數小于2/3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】指出下列反應中SiO2所表現的化學性質或作用,在A~E選項中選擇正確答案填入括號內。
①SiO2+2NaOH===Na2SiO3+H2O
②SiO2+2C===Si+2CO↑
③SiO2+3C===SiC+2CO↑
④SiO2+4HF===SiF4↑+2H2O
a.作為玻璃的成分被消耗而使玻璃被腐蝕
b.氧化性
c.酸性氧化物的通性
d.未參加氧化還原反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】金屬材料在日常生活以及生產中有著廣泛的運用。下列關于金屬的說法不正確的是( )
A.合金的性質與其成分金屬的性質不完全相同
B.工業上金屬Mg、Al都是用電解熔融的氯化物制得的
C.金屬冶煉的本質是金屬陽離子得到電子變成金屬原子
D.越活潑的金屬越難冶煉,冶煉方法與其活潑性有關
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com