
【題目】(1)海水淡化的方法主要有:__________、______________、_____________。
(2)金屬冶煉的實質是金屬化合物中的金屬離子得電子被________(填“氧化”或“還原”)為金屬單質的過程,寫出冶煉金屬鈉的化學方程式:_________________________。
(3)實驗室里,常用加熱銨鹽和堿的混合物的方法制氨,寫出實驗室制氨的化學方程式:________;氨溶于水得氨水,氨水呈___________性(填“酸”或“堿”); 密度比水_______;(填“大”或“小”)寫出向AlCl3溶液中滴加過量氨水的離子方程式:_________________________。
(4)溴主要以Br-形式存在于海水中,工業上制備的Br2的操作步驟為:
①一定條件下,將Cl2通入濃縮的海水中,生成Br2
②利用熱空氣將Br2吹出,并用濃Na2CO3溶液吸收,生成NaBr、NaBrO3等
③用硫酸酸化步驟②得到的混合物。
Br2可用熱空氣吹出,其原因是:_________;步驟③所發生的化學反應方程式為:_______________。
【答案】蒸餾法電滲析法離子交換法還原 2NaCl(熔融)![]() 2Na+Cl2↑2NH4Cl+Ca(OH)2
2Na+Cl2↑2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O堿小Al3++3NH3·H2O = Al(OH)3↓+3NH4+溴的沸點較低,易揮發5NaBr+NaBrO3+3H2SO4=3Na2SO4+3Br2+3H2O
CaCl2+2NH3↑+2H2O堿小Al3++3NH3·H2O = Al(OH)3↓+3NH4+溴的沸點較低,易揮發5NaBr+NaBrO3+3H2SO4=3Na2SO4+3Br2+3H2O
【解析】
海水淡化的常用方法有海水凍結法、電滲析法、蒸餾法、離子交換法;金屬冶煉的實質其實就是把金屬從化合態變為游離態,用還原的方法使金屬化合物中的金屬陽離子得電子變成金屬原子,原理就是利用氧化還原反應原理在一定條件下用還原劑把金屬礦石中的金屬離子還原成金屬單質;實驗室用消石灰與氯化銨共熱的方法制備氨氣,氨氣溶于水溶液呈堿性,密度比水小;溴易揮發,可用熱空氣吹出;NaBr、NaBrO3在酸性條件下可發生氧化還原反應生成溴單質。
(1)淡化海水,應將水與海水中的鹽進行分離,常用方法有蒸餾、電滲析以及離子交換法等。(2)金屬冶煉的實質其實就是把金屬從化合態變為游離態,用還原的方法使金屬化合物中的金屬陽離子得電子變成金屬原子,工業上用電解熔融的氯化鈉冶煉金屬鈉,反應的化學方程式為:2NaCl(熔融)![]() 2Na+Cl2↑。(3)實驗室用消石灰與氯化銨共熱的方法制備氨氣,消石灰與氯化銨共熱生成氯化鈣、氨氣和水,反應的化學方程式為:2NH4Cl+Ca(OH)2
2Na+Cl2↑。(3)實驗室用消石灰與氯化銨共熱的方法制備氨氣,消石灰與氯化銨共熱生成氯化鈣、氨氣和水,反應的化學方程式為:2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O;氨氣溶于水溶液呈堿性,氨水密度比水小;氨水與氯化鋁溶液反應生成氫氧化鋁沉淀和氯化銨溶液,反應的離子方程式為:Al3++3NH3·H2O = Al(OH)3↓+3NH4+。(4)海水提溴時,溴的沸點較低,易揮發,可用熱空氣吹出;NaBr、NaBrO3在酸性條件下可發生氧化還原反應生成溴單質,反應的化學方程式為5NaBr+NaBrO3+3H2SO4=3Na2SO4
CaCl2+2NH3↑+2H2O;氨氣溶于水溶液呈堿性,氨水密度比水小;氨水與氯化鋁溶液反應生成氫氧化鋁沉淀和氯化銨溶液,反應的離子方程式為:Al3++3NH3·H2O = Al(OH)3↓+3NH4+。(4)海水提溴時,溴的沸點較低,易揮發,可用熱空氣吹出;NaBr、NaBrO3在酸性條件下可發生氧化還原反應生成溴單質,反應的化學方程式為5NaBr+NaBrO3+3H2SO4=3Na2SO4
+3Br2+3H2O。
【題型】填空題
【結束】
27
【題目】一瓶未知溶液,其中可能含有H+、NH4+、K+、Na+、Mg2+、Ba2+、Fe3+、SO42-、CO32-、Cl-和I-。取該溶液進行了以下實驗:
(1)用pH試紙檢驗,表明溶液呈強酸性;
(2)取部分溶液,加入數滴氯水及2 mL CCl4,經振蕩后CCl4層呈紫紅色;
(3)另取部分溶液,加入NaOH 溶液使其變為堿性,無沉淀生成;
(4)取部分上述堿性溶液,加Na2CO3溶液,有白色沉淀生成;
(5)將(3)得到的堿性溶液加熱,有氣體放出,該氣體能使濕潤的紅色石蕊試紙變藍;
根據上述實驗事實,可知原溶液中肯定含有的離子是_________;肯定沒有的離子是_______________。
科目:高中化學 來源: 題型:
【題目】硫酸鋅可用于制造鋅鋇白、印染媒染劑等。用鋅白礦(主要成分為ZnO,還含有FeO、CuO、SiO2等雜質)制備ZnSO4·7H2O的流程如下。
已知:Ksp[Fe(OH)3]=4.0×1038,Ksp[Cu(OH)2]=2.2×1020

(1)“濾渣1”的主要成分是_______(填化學式)。“酸浸”過程中,為了提高鋅元素浸出速率,可采取的措施有:①適當提高酸的濃度,②_______(填一種)。
(2)“氧化”過程中,發生氧化還原反應的離子方程式是_______。
(3)“沉淀”過程中,加入ZnO產生Fe(OH)3沉淀的原因是_______。
(4)加入適量ZnO固體,若只析出Fe(OH)3沉淀而未析出Cu(OH)2沉淀,且測得沉淀后的溶液中c(Fe3+)=4.0×1014mol/L,此時溶液中c(Cu2+)的取值范圍是_______mol/L。
(5)加入適量鋅粉的作用是_______。
(6)由濾液得到ZnSO47H2O的操作依次為_______、_______、過濾、洗滌、干燥。實驗室中過濾操作需要使用的玻璃儀器有燒杯、_______、_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是( )
A. 化學平衡正向發生移動時,平衡常數K值一定增大
B. HS-的電離方程式:HS-+H2O![]() S2-+H3O+
S2-+H3O+
C. 由水電離出的c(H+)=1×10-13mol/L的溶液中,可能大量共存的離子:Fe3+、K+、NH4+、 SO42-、Cl-、ClO-
D. AlCl3溶液與Na2CO3溶液混合發生反應:2Al3++3CO32-=Al2(CO3)3↓
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】馬日夫鹽(Mn(H2PO4)2)是一種白色晶體,易溶于水,常用于機械設備的磷化處理。以軟錳礦(主要成分為MnO2,還含有少量的Fe2O3、FeO和Al2O3)為原料制備馬日夫鹽的流程如下:
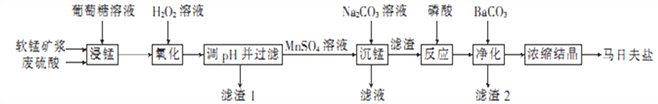
(1)粉碎軟錳礦制成礦漿的目的是_________________________________________,葡萄糖(C6H12O6)與MnO2反應時,產物為MnSO4、CO2和H2O,該反應中氧化劑與還原劑的物質的量之比為__________。
(2)用H2O2溶液“氧化”時發生反應的離子方程式為_______________________________。
(3)已知幾種金屬離子的氫氧化物開始沉淀和完全沉淀的pH如下表所示、“調pH并過濾”時,應調整的pH范圍為____________,濾渣1的主要成分為_________(填化學式)。
金屬離子 | 開始沉淀的pH | 完全沉淀的pH |
Fe3+ | 1.8 | 3.2 |
Al3+ | 3.0 | 5.0 |
Fe2+ | 5.8 | 8.8 |
Mn2+ | 7.8 | 9.8 |
(4)加入磷酸后發生反應的化學方程式為_____________________________________。
(5)某工廠用上述流程制備馬日夫鹽,已知軟錳礦中MnO2的含量為87%,整個流程中錳元素的損耗率為9%,則1t該軟錳礦可制得馬日夫鹽__________t。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖,鐵片、銅片和CuSO4溶液可以構成原電池或電解池,下列說法正確的是( )

A. 構成原電池時,Cu極反應式為Cu-2e-=Cu2+
B. 構成電解池時,Cu極質量可能減少也可能增加
C. 構成電解池時,Fe極質量一定減少
D. 構成的原電池或電解池在工作時的反應原理一定不同
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示,將甲、乙兩個裝有不同物質的針筒用導管連接起來,將乙針筒內的物質壓到甲針筒內,進行下表所列的不同實驗(氣體在同溫同壓下測定)。
![]()
實驗序號 | 甲針筒內物質 | 乙針筒內物質 | 甲針筒的現象 |
1 | 10 mLFeSO4溶液 | 10 mLNH3 | 生成白色沉淀,后變色 |
2 | 20 mLH2S | 12mLSO2 | |
3 | 30 mLNO2 | 10 mLH2O(l) | 剩有無色氣體,活塞自動向內壓縮 |
4 | 15 mLCl2 | 40 mLNH3 |
試回答下列問題:
(1)實驗1中,沉淀最終變為_____色,寫出沉淀變色的化學方程式_________________________。
(2)實驗2甲針筒內的現象是:有_____________生成,活塞______移動(填向外、向內、不)。
反應后甲針筒內有少量的殘留氣體,正確的處理方法是將其通入___________溶液中。
(3)實驗3中,甲中最后剩余的無色氣體是_______,寫出NO2與H2O反應的化學方程式_______。
(4)實驗4中,已知:Cl2 + NH3 → N2+ HCl。甲針筒除活塞有移動,針筒內有白煙產生外,氣體的顏色變化為____________,最后針筒中剩余氣體的體積約為_________mL。
【答案】紅褐色4Fe(OH)2+O2+2H2O=4Fe(OH)3淡黃色固體向內NaOHNO3NO2+H2O = 2HNO3+NO黃綠色變為無色5
【解析】
+2價的鐵離子易被氧氣氧化成+3價的鐵離子,NH3與FeSO4溶液的水反應生成Fe(OH)2沉淀,Fe(OH)2沉淀易被空氣中的氧氣氧化;H2S和SO2反應生成單質硫和水,過量的SO2用堿吸收;NO2與水反應生成硝酸和一氧化氮;氯氣的顏色為黃綠色,氨氣與氯氣發生氧化還原反應生成氮氣和氯化氫,3Cl2+2NH3═N2+6HCl,過量的氨氣與產物氯化氫反應生成氯化銨。
(1)氨氣溶于水得到氨水,反應的化學方程式為:NH3+H2ONH3H2O,氨水與硫酸亞鐵溶液反應生成氫氧化亞鐵白色沉淀,反應的化學方程式為:FeSO4+2NH3H2O═Fe(OH)2↓+(NH4)2SO4,Fe(OH)2白色沉淀,在空氣中易被空氣中的氧氣氧化,迅速變成灰綠色,最終變為紅褐色,反應的化學方程式為:4Fe(OH)2+O2+2H2O═4Fe(OH)3。(2)15mLH2S和10mLSO2反應2H2S+SO2=3S+2H2O,反應產生固體硫和液態水,SO2過量,針筒內壓強減小,活塞自動向內移動,析出淺黃色固體,過量的SO2用NaOH溶液吸收。(3)二氧化氮氣體溶于水,與水反應生成硝酸和一氧化氮,反應的化學方程式為:3NO2+H2O=2HNO3+NO,由方程式可知可知30 mLNO2生成10mL無色的NO氣體。(4)氯氣的顏色為黃綠色,氨氣與氯氣發生氧化還原反應生成氮氣和氯化氫,氣體顏色變淺,反應的化學方程式為:3Cl2span>+2NH3═N2+6HCl,由方程式可知,15 mLCl2消耗10ml氨氣、生成30ml氯化氫,過量的氨氣與氯化氫恰好反應生成氯化銨,反應中有大量的白煙產生。
【點睛】
該題主要考查了元素及其化合物的知識,涉及氮、氯、硫的化合物的性質,注意根據化合物的性質認識理解化學反應,正確分析實驗現象。
【題型】填空題
【結束】
30
【題目】有一瓶硫酸和硝酸的混合溶液(1)取出10.00mL該溶液,加入足量BaCl2溶液,過濾、洗滌、干燥得4.66g沉淀。濾液跟40 mL 2.00mol/L的NaOH溶液恰好反應使溶液呈中性,則混合液中硫酸和硝酸的物質的量濃度分別為多少____?(2)取出20.00mL該溶液,加入足量Cu粉,若氧化產物只有NO,可產生NO的物質的量是多少____ ?
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】己知:I2+2S2O32-=S4O62-+2I-。相關物質的溶度積常數見下表:
物質 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
Ksp | 2.2×10-20 | 2.6×l0-39 | 1.7×l0-7 | 1.3×l0-12 |
(1)某酸性CuCl2溶液中含有少量的FeCl3,為得到純凈的CuC12·2H2O晶體,常加入CuO或Cu(OH)2,調至pH=4,使溶液中的Fe3+轉化為Fe(OH)3沉淀,此時溶液中的c(Fe3+)=_____________。 過濾后,將所得濾液低溫蒸發、濃縮結晶,可得到CuCl2·2H2O晶體。
(2)在空氣中直接加熱CuCl2·2H2O晶體得不到純的無水CuC12, 原因是(用化學方程式表示)_____________________________,由CuCl2·2H2O晶體得到純凈的無水CuCl2的合理方法是________________________________________________。
(3)某學習小組用“間接碘量法”測定含有CuCl2·2H2O晶體的試樣(不含能與I-發生反應的氧化性雜質)的純度,過程如下:取1.44g試樣溶于水,加入過量KI固體,充分反應,生成白色沉淀(CuI)。將反應后的溶液稀釋為100 mL,用0.1000mol/LNa2S2O3標準溶液(溶液呈弱堿性)進行滴定,滴定結果如下表所示。
滴定次數 | 待測溶液的體積/mL | 標準溶液的體積/mL | |
滴定前刻度 | 滴定后刻度 | ||
1 | 25.00 | 0.02 | 22.03 |
2 | 25.00 | 2.00 | 21.98 |
3 | 25.00 | 0.20 | 20.22 |
①可選用__________作滴定指示劑,滴定終點的現象是_________________________。
②滴定過程中操作滴定管的圖示正確的是_____________。
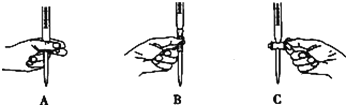
③若滴定時出現下列情況,測定結果偏高的是___________。
a.滴定前用蒸餾水沖洗錐形瓶 b.滴定前滴定管尖嘴有氣泡,滴定后氣泡消失
c.酸式滴定管滴至終點時俯視讀數 d.酸式滴定管用蒸水洗后,未用標準液潤洗
④CuCl2溶液與KI反應的離子方程式為______________________________。
⑤該試樣中CuCl2·2H2O的質量百分數為____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】安全是順利進行實驗及避免傷害的保障.下列實驗操作正確且不是從實驗安全角度考慮的是( )

A. 操作①:使用稍浸入液面下的倒扣漏斗檢驗氫氣的純度
B. 操作②:使用CCl4萃取溴水中的溴時,振蕩后需打開活塞使漏斗內氣體放出
C. 操作③:吸收氨氣或氯化氫氣體并防止倒吸
D. 操作④:用食指頂住瓶塞,另一只手托住瓶底,把瓶倒立,檢查容量瓶是否漏水
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com