
【題目】(13分)由乙烯和其它無機原料合成環狀酯E和高分子化合物H的示意圖如下:

請回答下列問題:
(1)寫出結構簡式:A F C
(2)反應類型:X 、Y
(3)寫出化學反應方程式:
A→B
G→H
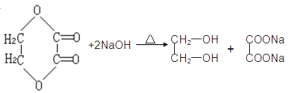
(4)若環狀酯E在NaOH溶液中共熱,則發生反應的化學方程式為:
【答案】(1)A:CH2BrCH2Br F:CH≡CH, C:OHC—CHO(每空1分)
(2)X:酯化反應 Y:加聚反應 (3)A→B:![]()
G→H:![]()
【解析】乙烯含有碳碳雙鍵,能和溴水發生加成反應,生成1,2-二溴乙烷,即A的結構簡式為CH2BrCH2Br。A在氫氧化鈉的醇溶液中發生消去反應生成F,則F是乙炔。乙炔和氯化氫發生加成反應生成G,則G是CH2=CHCl。G中含有碳碳雙鍵,能發生加聚反應生成高分子化合物H,則H是聚氯乙烯。A也能在氫氧化鈉的水溶液中發生水解生成B,則B是乙二醇。乙二醇氧化生成C,則C是乙二醛。乙二醛繼續被氧化生成乙二酸。乙二酸和乙二醇發生酯化反應生成環酯E。


 培優口算題卡系列答案
培優口算題卡系列答案 開心口算題卡系列答案
開心口算題卡系列答案 口算題卡河北少年兒童出版社系列答案
口算題卡河北少年兒童出版社系列答案 A加金題 系列答案
A加金題 系列答案科目:高中化學 來源: 題型:
【題目】聚酯增塑劑廣泛用于耐油電纜、煤氣管、防水卷材、鞋料、室內高級裝飾品、耐油耐汽油的特殊制品等。聚酯增塑劑G及某醫藥中間體N的一種合成路線如下(部分反應條件略去):

已知:
(1)
(2)CH3CH=CHCH2CH3![]() CH3COOH+CH3CH2COOH
CH3COOH+CH3CH2COOH
請回答下列問題:
(1)N中官能團的名稱為________;反應②的試劑和條件是:__________;
(2)反應⑤的反應類型是________,反應⑧的反應類型是____________;
(3)I的結構簡式為____________;
(4)寫出B與H反應生成聚酯增塑劑G的化學方程式__________;
(5)H的同分異構體滿足下列條件的共有______種(不含立體異構)
①1mol該物質能與2molNaOH溶液反應
②1mol該物質與銀氨溶液反應生成4molAg
③有且只有2個甲基
其中核磁共振氫譜顯示位組峰,且峰面積比為3:1:2的是________(寫出一種結構簡式)
(6)參考以上合成路線的信息,設計一條以苯甲酸和乙醇為原料合成![]() 的路線(無機試劑任選,需注明反應條件):_________。
的路線(無機試劑任選,需注明反應條件):_________。
示例:原料![]() …產物
…產物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用接觸法制5t98%的濃硫酸,在理論上需要含FeS2 75%(雜質不含硫元素)的硫鐵礦為 ( )
A. 4.3t B. 8t C. 4t D. 5.6t
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】堿性鋅錳電池是日常生活中消耗量最大的電池,其構造如圖所示。
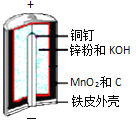
放電時總反應為:Zn + 2H2O + 2MnO2![]() Zn(OH)2 + 2MnOOH
Zn(OH)2 + 2MnOOH
從廢舊堿性鋅錳電池中回收Zn和MnO2的工藝如下:
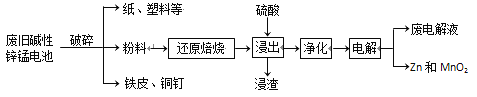
回答下列問題:
(1)MnOOH中,Mn元素的化合價為________。
(2)“還原焙燒”過程中,高價金屬化合物被還原為低價氧化物或金屬單質(其中MnOOH、MnO2被還原成MnO),主要原因是“粉料”中含有________。
(3)“凈化”是為了除去浸出液中的Fe2+,方法是:加入________(填化學式)溶液將Fe2+氧化為Fe3+,再調節pH使Fe3+完全沉淀。(離子濃度小于1×10-5mol·L-1即為沉淀完全)已知浸出液中Mn2+、Zn2+的濃度約為0.1 mol·L-1,根據下列數據計算調節pH的合
理范圍是________至________。
化合物 | Mn(OH)2 | Zn(OH)2 | Fe(OH)3 |
KSP近似值 | 10-13 | 10-17 | 10-38 |
(4)“電解”時,陽極的電極反應式為_____。本工藝中應循環利用的物質是_____(填化學式)。
(5)若將“粉料”直接與鹽酸共熱反應后過濾,濾液的主要成分是ZnCl2和MnCl2。“粉料”中的MnOOH與鹽酸反應的化學方程式為________。
(6)某堿性鋅錳電池維持電流強度0.5A(相當于每秒通過5×10-6 mol電子),連續工作80分鐘即接近失效。如果制造一節電池所需的鋅粉為6 g,則電池失效時仍有________%的金屬鋅未參加反應。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是()
A. 2015年8月12日,天津濱海新區某公司的倉庫發生爆炸,事發倉庫里存放了大量的硝酸銨、氰化鈉、電石和金屬鈉等危險化學品這四種藥品均屬于電解質
B. 纖維素、蔗糖、葡萄糖和脂肪在一定條件下都可發生水解反應
C. 氮氧化物對環境有很大危害,如破壞臭氧層,形成酸雨,產生光化學煙霧等
D. 工業上利用氯氣與澄清石灰水反應制取漂白粉
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學與生產、生活、社會發展等息息相關。下列說法正確的是( )
A. 做衣服的棉、麻、絲綢灼燒有燒焦羽毛的氣味
B. 糖尿病人應少吃含糖類的食品,可常喝糯米八寶粥
C. 現代工業生產中的芳香烴來源于石油的催化重整和煤的干餾
D. 豆漿中富含大豆蛋白,煮沸后蛋白質即水解生成氨基酸
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】三氯化硼的熔點為-107.3 ℃,沸點為12.5 ℃,易水解生成硼酸(H3BO3),可用于制造高純硼、有機合成催化劑等。實驗室制取三氯化硼的原理為B2O3+3C+3Cl2![]() 2BCl3+3CO。
2BCl3+3CO。
(1)甲組同學擬用下列裝置制取純凈干燥的氯氣(不用收集)。

①裝置B中盛放的試劑是__,裝置C的作用是___________________。
②裝置A中發生反應的離子方程式為 _____________________________。
(2)乙組同學選用甲組實驗中的裝置A、B、C和下列裝置(裝置可重復使用)制取BCl3并驗證反應中有CO生成。
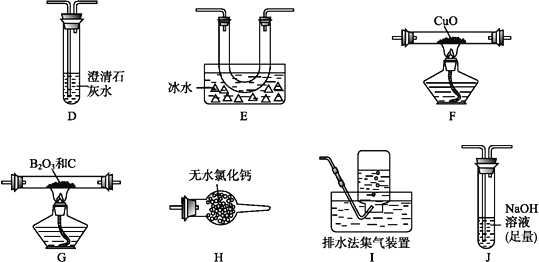
①乙組同學的實驗裝置中,依次連接的合理順序為
A→B→C→G→__→__→__→__→F→D→I。
②能證明反應中有CO生成的現象是___________________________。
③開始實驗時,先點燃____(填“A” 或“G”)處的酒精燈。
④請寫出BCl3水解的化學方程式__________________________。
⑤硼酸是一元弱酸,其鈉鹽化學式為Na [B(OH)4],則硼酸在水中電離方程式是____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ.寫出下列反應的離子方程式:
(1)將雞蛋殼在醋酸中溶解有氣泡產生:_____________________________________________;
(2)CuSO4溶液與Ba(OH)2溶液混合:________________________________________。
Ⅱ.對一份稀溶液作初步分析后發現,溶液無色、澄清,其可能含有![]() 、Na+、
、Na+、![]() 、H+、
、H+、![]() 、
、![]() 、Cl等離子中的若干種。然后又作了如下分析,以確定這些離子是否存在。
、Cl等離子中的若干種。然后又作了如下分析,以確定這些離子是否存在。
①用石蕊試液檢測該溶液時,溶液顯紅色。
②取2 mL溶液用BaCl2溶液和稀硝酸進行檢驗,結果生成了白色沉淀。
③對②中所得的混合物充分靜置后,取其上層澄清的液體用AgNO3溶液和稀硝酸進行檢驗,結果又生成了白色沉淀。
請回答下列問題:
(1)原溶液中一定存在的離子是__________,一定不存在的離子是____________。
(2)在上述實驗操作中,有錯誤的步驟是(填代號)______。對該錯誤改正的方法是(要作較詳細的說明)_________________________________________________________。
(3)到目前為止,不能肯定在原溶液中是否存在的離子是____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關說法正確的是 ( )
A. 1mol NaCl分子中含有1mol Na+和1mol Cl-
B. 離子化合物和共價化合物溶于水都能導電
C. 離子鍵的形成一定有電子的得失
D. KOH溶于水電離出K+ 和OH- 不是化學變化
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com