
���}Ŀ�����Ќ����Ҫ�x����ԇ�����x�����_(d��)�����?z��i)��ĵ��?/span>
�x� | ��Ҫ�x�� | ԇ�� | ���?z��i)��?/span> |
A | ��ƿ���L�i©�����ƾ�������(d��o)�� | ܛ�i�V�c���}�� | ��ȡ���ռ�������Ț� |
B | �ƾ����������������l(f��)�����_�� |
| ���l(f��)��Һ�õ����w |
C | �A�ן�ƿ����(d��o)��ܡ��������F���_ | ����İ��⡢ˮ | ģ�M��Ȫ��� |
D | �F�z���{(l��n)ɫ⒲������ƾ��� | �}�ᡢ���yҺ | ��ɫ����(y��ng)��� |
A.AB.BC.CD.D
���𰸡�A
��������
A.��ȡ���ռ�������Ț⣬��(y��ng)����ȡ���Ț��M(j��n)�г��s�����߀��Ҫϴ��ƿ���ʳ�}ˮ�͝����ᣬ�������L�i©��������÷�Һ©������A�����_(d��)�����?z��i)��ģ?/span>
B.���l(f��)![]() ��Һ���Ȼ��c���w����Ҫ�ƾ����������������l(f��)�����_�ܣ�B���_(d��)�����?z��i)��ģ?/span>
��Һ���Ȼ��c���w����Ҫ�ƾ����������������l(f��)�����_�ܣ�B���_(d��)�����?z��i)��ģ?/span>
C.ģ�M��Ȫ����Ҫ�A�ן�ƿ����(d��o)��ܡ��������F���_������İ��⡢ˮ��C���_(d��)�����?z��i)��ģ?/span>
D.���F�zպϡ�}���ڟoɫ�������Ɵ����oɫ��պȡԇ���ڟoɫ�������Ɵ��^������ɫ�����z��Ҫ�^�{(l��n)ɫ⒲����^�죬D���_(d��)�����?z��i)��ģ?/span>
���xA��



| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ������Ȳ��(d��o)늾ۺ���ĺϳ�ʹ�߷��Ӳ����M(j��n)�������ϳɽ�������������ӌW(xu��)�r������(d��ng)�� ��Ȳ���ӎ���ˎ�������ȷ���Ƭ�κ;�����һ����������ԡ��������҇����W(xu��)�� ������ϳɵľ���Ȳ��������� M �ĽY(ji��)��(g��u)ʽ�� M ��ϡ���������µ�ˮ���^�̡�
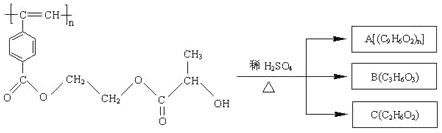
�������P(gu��n)�f���������_����
A. M �c A ����ʹ���Ը��i�����Һ����ˮ��ɫ
B. B �к��ЃɷN���܈F(tu��n)��B �ܰl(f��)����ȥ����(y��ng)�Ϳs�۷���(y��ng)
C. A��B��C �� 1 mol �քe�����������c����(y��ng)���ų��Ě��w�����|(zh��)����֮�Ȟ� 1��2��2
D. 1 mol M �c��ğ��A��Һ����(y��ng)�������� 2n mol �� NaOH
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ�����W(xu��)����(y��ng)�е�����׃�����ɻ��W(xu��)����(y��ng)���f���W(xu��)�I���ѕr���յ������c�»��W(xu��)�I�γɕr�ų���������ͬ����ģ���D��N2(g)��O2(g)����(y��ng)����NO(g)�^���е�����׃�����t�����f�����_���ǣ� ��
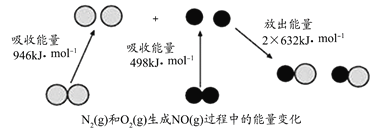
A.ͨ����r�£�NO��N2��(w��n)��
B.ͨ����r�£�N2(g)��O2(g)�����ֱ������NO
C.1molN2(g)��1molO2(g)����(y��ng)���յ�������180kJ
D.1molN2(g)��1molO2(g)���еĿ���������2molNO(g)���еĿ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ��Ni(CO)4�������ЙC(j��)�ϳɣ�Ҳ������������һ���l���£�һ���ݷe�����]�����У��l(f��)������(y��ng)��Ni(s)+4CO(g)![]() Ni(CO)4(g)����֪ԓ����(y��ng)ƽ�ⳣ��(sh��)�c�ضȵ��P(gu��n)ϵ���±���
Ni(CO)4(g)����֪ԓ����(y��ng)ƽ�ⳣ��(sh��)�c�ضȵ��P(gu��n)ϵ���±���
�ض�/�� | 25 | 80 | 230 |
ƽ�ⳣ��(sh��) | 5��104 | 2 | 1.9��10-5 |
�����f�����_����
A. 25���_(d��)��ƽ��r�����������^�m(x��)ͨ��CO��Ni���D(zhu��n)��������CO�D(zhu��n)���ʜpС
B. �ض�Խ�ͣ�Խ������Ni(CO)4�����a(ch��n)
C. ��80��r���y��ij�r�̣�Ni(CO)4��CO��Ⱦ���0.5mol/L���t�˕rv(��)��v(��)
D. ƽ��r�����]�����м�������懷ۣ�ƽ����������(y��ng)�����Ƅӣ���ƽ��rCO��ȱ�ԭƽ��С
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ�����и���(j��)����(y��ng)ԭ���O(sh��)Ӌ�đ�(y��ng)�ã������_����
A. CO32����H2O![]() HCO3����OH������ļ��A��Һ��ϴ����
HCO3����OH������ļ��A��Һ��ϴ����
B. Al3����3H2O![]() Al(OH)3��3H�������\��ˮ
Al(OH)3��3H�������\��ˮ
C. TiCl4��(x��2)H2O(�^��) ![]() TiO2��xH2O����4HCl����TiCl4�Ƃ�TiO2
TiO2��xH2O����4HCl����TiCl4�Ƃ�TiO2
D. SnCl2��H2O![]() Sn(OH)Cl����HCl�������Ȼ����a��Һ�r����������c
Sn(OH)Cl����HCl�������Ȼ����a��Һ�r����������c
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ������N2O5����������һ�N���͵ľGɫ�������g(sh��)���ں��ܲ��ϡ��t(y��)ˎ�ȹ��I(y��)�еõ��V����(y��ng)�á��ش����І��}
��1��1840�� Devil�ø�����Ț�ͨ�^����������y���õ�N2O5��ԓ����(y��ng)�������a(ch��n)����һ�N���w�������ʽ��___________��
��2��F. Daniels�������Üy�����ڄ��Է���(y��ng)�����о���25��rN2O5(g)�ֽⷴ��(y��ng)��
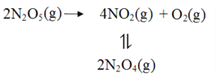
����NO2���۞�N2O4�ķ���(y��ng)����Ѹ���_(d��)��ƽ�⡣�wϵ�Ŀ�����(qi��ng)p�S�r�gt��׃�����±���ʾ��t=�ޕr��N2O4(g)��ȫ�ֽ⣩��
t/min | 0 | 40 | 80 | 160 | 260 | 1300 | 1700 | �� |
p/kPa | 35.8 | 40.3 | 42.5. | 45.9 | 49.2 | 61.2 | 62.3 | 63.1 |
����֪��2N2O5(g)��2N2O4(g)+O2(g) ��H1=4.4 kJ��mol1
2NO2(g)��N2O4(g) ��H 2=55.3 kJ��mol1
�t����(y��ng)N2O5(g)��2NO2(g)+ ![]() O2(g)�Ħ�H=_______ kJ��mol1��
O2(g)�Ħ�H=_______ kJ��mol1��
���о�������N2O5(g)�ֽ�ķ���(y��ng)����![]() ��t=62 min�r���y���wϵ��
��t=62 min�r���y���wϵ��![]() pO2=2.9 kPa���t�˕r��
pO2=2.9 kPa���t�˕r��![]() =________kPa��v=_______kPa��min1��
=________kPa��v=_______kPa��min1��
������߷���(y��ng)�ض���35�棬�tN2O5(g)��ȫ�ֽ���wϵ����(qi��ng)p��(35��)____63.1 kPa������ڡ������ڡ���С�ڡ�����ԭ����________��
��25��rN2O4(g)![]() 2NO2(g)����(y��ng)��ƽ�ⳣ��(sh��)Kp=_______kPa��Kp���Է։���ʾ��ƽ�ⳣ��(sh��)��Ӌ��Y(ji��)������1λС��(sh��)����
2NO2(g)����(y��ng)��ƽ�ⳣ��(sh��)Kp=_______kPa��Kp���Է։���ʾ��ƽ�ⳣ��(sh��)��Ӌ��Y(ji��)������1λС��(sh��)����
��3�����ڷ���(y��ng)2N2O5(g)��4NO2(g)+O2(g)��R.A.Ogg������·���(y��ng)�v�̣�
��һ�� N2O5![]() NO2+NO3 ����ƽ��
NO2+NO3 ����ƽ��
�ڶ��� NO2+NO3��NO+NO2+O2 ������(y��ng)
������ NO+NO3��2NO2 �췴��(y��ng)
���пɽ����J(r��n)��ڶ�������(y��ng)��Ӱ푵�һ����ƽ�⡣���б������_����_______�����(bi��o)̖)��
A��v(��һ�����淴��(y��ng))��v(�ڶ�������(y��ng))
B������(y��ng)�����g�a(ch��n)��ֻ��NO3
C���ڶ�����NO2�cNO3����ײ�H������Ч
D������������(y��ng)����^��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ��������Ԫ��X��Y��Z��W��Qԭ����(sh��)����������֪��X���������Ӕ�(sh��)�Ǵ���ӵ�2�����ڵؚ���Z�ĺ������W�Ƕ�����Ԫ����ԭ�Ӱ돽��������Ԫ�أ�Q������ӱȴ������2����ӡ�Ո�ش����І��}��
��1��X�ăr������Ų�ʽ��___��Q��ԭ�ӽY(ji��)��(g��u)ʾ��D��____��
��2��Y��Z�ɷNԪ���У���һ��x���^����ǣ���Ԫ�ط�̖��_____��ԭ����______��
��3��Z��W��Q���NԪ�صĺ����x�ӵİ돽��С�������е���________��
��4���P(gu��n)��Y��Z��Q���NԪ�ص��������P(gu��n)�f�������_����_______��
A.Y��܉����ʾʽ�ǣ�
B.Z��Q�ɷNԪ�صĺ��Κ仯��ķ�(w��n)�����^��(qi��ng)����Z
C. Z��Q�ɷNԪ�غ��Κ仯��ķ��c�^�ߵ���Q
D.Y��Ҋ���|(zh��)�Ц��I�c���I�Ĕ�(sh��)Ŀ֮����1��2
��5��Q�cZ�γɵĻ�����QZ2������ԭ��Q���s�������_____��QZ2������ˮ��ԭ����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ�����I(y��)�U�⡢��܇β���ŷų���SO2��NOx�ȣ����γ��F������Ҫ���������ɿ՚��еĻ҉m�����ᡢ���ᡢ�ЙC(j��)̼?x��)仯����������γɵğ��F��
(1) SO2��NOx�ڿ՚��д�������ƽ�⣺
2NO(g)��O2(g)![]() 2NO2(g) ��H=��113.0kJ��mol��1
2NO2(g) ��H=��113.0kJ��mol��1
2SO2(g)��O2(g)![]() 2SO3(g) ��H=��196.6kJ��mol��1
2SO3(g) ��H=��196.6kJ��mol��1
SO2ͨ���ڶ��������Ĵ����£��M(j��n)һ��������������SO3��
�ٌ���NO2��SO2����(y��ng)�ğữ�W(xu��)����ʽ��________________________________________��
���S�ض����ߣ�ԓ����(y��ng)���W(xu��)ƽ�ⳣ��(sh��)׃��څ����______(���������������pС��������׃���������ܴ_����)��
(2)���I(y��)�������ȉA���I(y��)�a(ch��n)Ʒ��������������ďU����D���ȉA���I(y��)��늽��ʳ�}ˮ��ԭ��ʾ��D
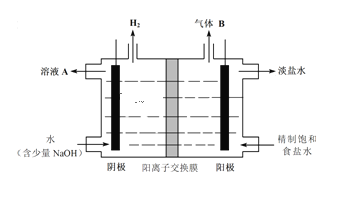
��늽��ʳ�}ˮ�Ļ��W(xu��)����ʽ��_______________________________________________��
������ҺA���պ���������ďU�⣬�䷴��(y��ng)���x�ӷ���ʽ��_______________________��
���ú����wB��Һ���պ���������ďU�⣬�䷴��(y��ng)���x�ӷ���ʽ��__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ��CuS��Cu2S����̎�����ԏUˮ�е�Cr2O72-������(y��ng)���£�
����(y��ng)��CuS��Cr2O72-��H����Cu2����SO42-��Cr3����H2O(δ��ƽ)��
����(y��ng)��Cu2S��Cr2O72-��H����Cu2����SO42-��Cr3����H2O(δ��ƽ)
�������P(gu��n)�f�����_����
A.����(y��ng)��͢��и���2�NԪ�صĻ��σr�l(f��)��׃��
B.����(y��ng)����߀ԭ���c�����������|(zh��)����֮�Ȟ�3��5
C.̎��1mol Cr2O72-�r����(y��ng)��������H�������|(zh��)�������
D.�|(zh��)����ͬ�r��Cu2S��ȥ�������Cr2O72-
�鿴�𰸺ͽ���>>
���H�W(xu��)У��(y��u)�x - ����(x��)���б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙�(qu��n)�e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com