
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
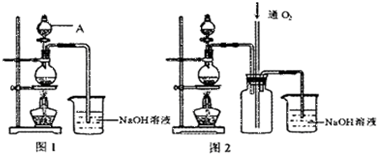
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
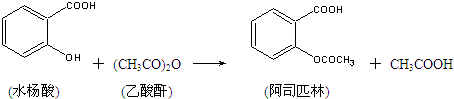
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
化學方程式練習
一、用化學方程式表示下列各種物質的實驗室制法
1、O2(三種方法):
2、H2:
3、Cl2:
4、NH3:
5、CO2:
6、NO:
二、用方程式表示工業生產過程(參考選修Ⅱ,帶*的寫離子方程式,注意反應條件)
1、氯堿工業(電解飽和食鹽水)
*陽極:
*陰極:
*總反應:
2、接觸法制硫酸(硫鐵礦為原料)
①沸騰爐: ;其中氧化產物為:
②接觸室: ;
V2O5的作用是 ,反應溫度控制在400~500℃的原因是
③吸收塔:
用98%H2SO4吸收SO3而不用水直接吸收的原因是
。
④尾氣處理:
3、海水提溴:
*①氯化:
②吹出
③吸收:
④轉化:
4、合成氨:
①由水和碳合成H2
②合成塔:
5、氨氧化制硝酸
①氧化爐:
②吸收塔:
③制取化肥硝酸銨:
6、冶煉鋁(冰晶石作熔劑)
①堿溶:
②沉淀:
③脫水:
④電解:*陽極:
*陰極:
總反應:
7、鋁熱法制鐵
8、由三氧化鎢制鎢
9、工業制漂白粉
10、制玻璃
11、工業生產石灰漿
12、聯合制堿法:
13、高純硅的生產
。
14、煉鐵煉鋼
①還原劑的生成:
;
②鐵的還原(將鐵的氧化物,如Fe2O3還原):
③將生鐵脫硫去磷降低含碳量即得鋼。
三、完成下列反應的化學方程式(注意寫反應條件)。
1、Fe + H2O(g)=
2、C+ H2O(g) =
3、CO+ H2O(g) =
4、F2+ H2O=
5、NH3+H2O
6、NO2+ H2O=
7、SO2+ H2O
8、Cl2 + H2O=
9、K + H2O=
10、Na2O2+ H2O=
11、CaC2+ H2O=
12、Mg3N2+ H2O =
13、Al + NaOH+ H2O=
14、CaCO3+ H2O+ CO2=
15、Fe(OH)2+ H2O+ O2=
16、FeCl3+ H2O
17、NH4Cl+H2O
18、Na2CO3+H2O
19、CuSO4+H2O電解
20、Na2S2O3 + HCl =
21、SiO2 + HF=
22、SiO2 + NaOH=
23、Na2SiO3+ HCl=
四、寫出下列物質分別與NaOH溶液反應的化學方程式。
1、Si
2、Cl2
3、SiO2
4、SO2 (足量)
5、CO2(小量)
6、H3PO4
7、H2SO4
8、CH3Br
9、Al
10、Al2O3
11、AlCl3
12、Al(OH)3
13、CuSO4
14、NaHCO3
15、Ca(HCO3)2(足量)
16、(NH4)2SO4
五、寫出下列物質受熱或光照的化學方程式。
1、NaHCO3
2、HNO3
3、AgBr
4、H2SO3
5、NH4HCO3
6、Cu(OH)2
7、Ca(HCO3)2
8、Cu2(OH)2CO3
9、H2O2
10、KClO3
11、KMnO4
12、NH4Cl
13、HClO
14、CH4+Cl2
15、H2+Cl2
16、CuO
六、寫出下列反應的化學方程式和離子方程式
1、SO2使溴水褪色:
2、SO2使酸性高錳酸鉀溶液褪色:
3、氫氧化鐵溶于氫碘酸:
4、乙二酸(草酸)使酸性高錳酸鉀溶液褪色 :
5、用石灰水與小蘇打溶液制燒堿:
6、硫酸氫銨與氫氧化鋇溶液混合:
7、漂白粉溶液中充入足量CO2:
8、KHSO4與氫氧化鋇溶液混合呈中性:
9、Fe3O4溶于稀硝酸:
10、明礬溶液中加Ba(OH)2溶液至沉淀量最大:
七、用離子方程式表示下列在溶液中的反應
1、KCl+AgNO3:
2、Ba(OH)2+H2SO4:
3、BaCO3+HCl:
4、Cu(OH)2+HCl:
5、Fe(OH)2+HNO3(稀) :
6、FeCl3+KSCN:
7、FeBr2+Cl2(物質的量之比為1:1):
8、NaBr+Cl2:
9、Fe+CuCl2:
10、Zn+AgNO3:
11、純堿水解:
12、明礬凈水:
13、銅和稀硝酸:
14、配制銀氨溶液:
15、Na2O2投入稀硫酸中:
八、寫出下列物質在空氣中變質的化學方程式
1、Na2SO3:
2、NaOH:
3、NO:
4、Na:
5、Na2O2:
6、銅生銹:
7、氯水:
8、白磷:
9、稀硫酸酸化的FeSO4溶液變棕黃色
10、無色KI溶液變棕黃色
11、漂白粉失效:
九、寫出下列反應的化學方程式
1、混合H2S和SO2生成硫和水:
2、炭加熱放入濃硫酸中:
3、乙醇催化氧化為乙醛:
4、乙醛與銀氨溶液反應:
5、乙醛與新制Cu(OH)2加熱:
6、銅與濃硫酸共熱:
7、氧化硫通入濃溴水:
8、銅與濃硝酸反應:
9、木炭和濃硝酸共熱:
10、FeCl3溶液中加入KI溶液:
11、高錳酸鉀固體中滴入濃鹽酸:
12、氨水通入少量SO2:
13、偏鋁酸鈉溶液中加足量稀硫酸:
14、NaAlO2溶液中充入足量CO2:
15、Ba(AlO2)2溶液中加入硫酸鋁溶液:
16、氫氧化亞鐵水溶液在空氣中變質:
12、氯化鐵溶液溶解銅:
十、按要求寫方程式
1、寫出高溫條件下發生的置換反應四個:
①
②
③
④
2、寫出一個點燃條件下的置換反應:
3、寫出一個加熱條件下的置換反應:
4、寫出一個有三種反應物的置換反應:
5、寫出工業生產中需要高溫條件的反應(不少于5個)的化學方程式:
6、試設計一個實驗,檢驗某溶液中存在Fe2+,請在下面的橫線上按操作順序寫出相應的離子方程式: 。
7、治療胃酸過多的藥物中常用Al(OH)3,如何用氧化鋁制取氫氧化鋁?要求制取過程中酸堿的用量降到最少。按生產順序寫出相關的離子方程式: 。
8、化學反應中有的具有相似性,有的反應具有特殊性,試寫出下列相關化學方程式,并思考其中的原因:
① Li + O2
Na + O2
② Mg + CO2
Mg + SO2
③ Na2O2 + CO2
Na2O2 + SO2
KO2 + CO2
④ F2 + H2O
Cl2 + H2O
⑤ Fe + Cl2
Fe + I2
⑥ Fe(OH)3 + HCl
Fe(OH)3 + HI
9、按要求寫化學方程式
①堿性氧化物與水反應(舉2例)
②堿性氧化物與酸反應(舉2例)
③金屬氧化物但不是堿性氧化物的氧化物與水反應(舉一例)
④酸性氧化物與水反應(舉2例,其中一例為金屬氧化物)
⑤能與水反應生成酸,但不是酸性氧化物也不是堿性氧化物氧化物與水反應的化學方程式:
。
⑥列舉不少于5類既能與強酸反應,又能與強堿反應的物質,并分別寫出它們與酸(HCl)、堿(NaOH)反應的離子方程式:
A、物質化學式:
B、物質化學式:
C、物質化學式:
D、物質化學式:
E、物質化學式:
F、物質化學式:
G、物質化學式:
10、某酸性氧化物,它能與某些酸反應,也能與堿反應,請寫出這樣的氧化物一種,并寫出它與酸反應的化學方程式和與堿反應的離子方程式:
氧化物分子式:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com