
【題目】某校化學學習小組利用如圖裝置來制取乙酸乙酯。
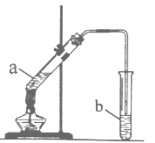
I.實驗過程:向試管a中加入碎瓷片,3mL乙醇,然后邊振蕩試管邊慢慢加入2mL濃硫酸,最后加入2mL乙酸,按圖連接好裝置,用酒精燈緩慢加熱,將產生的蒸汽經導管通到b試管中的液面上。
II. 已知化學方程式:CH3COOH+CH3CH2OH ![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
III.查閱資料得知:乙酸乙酯不溶于水,密度比水小,且有香味
請回答下列問題:
(1)試管a中加入碎瓷片,其作用是_____(填字母代號)。
A.加快化學反應速率 B.防止溶液暴沸
(2)試管b中的溶液是_____(填字母代號)。
A飽和碳酸鈉溶液 B.飽和氫氧化鈉溶液
(3)實驗完畢后,將b試管中的液體充分振蕩,靜置后,溶液分為兩層。
①乙酸乙酯在________(填“上層”或“下層”)。
②常用________操作將兩層液體分離(填“過濾”或“分液”)。
(4)實驗中加入乙酸的質量為2.1g,其中60%的乙酸發生酯化反應,則得到乙酸乙酯的質量為______g(計算結果保留兩位小數)。
【答案】B A 上層 分液 1.85
【解析】
根據實驗室制備乙酸乙酯的實驗原理及裝置分析解答;根據關系式計算產物的質量。
(1)液體乙酸乙醇沸點低,加熱要加碎瓷片,防止暴沸,故答案為:B;
(2)試管b中的溶液是飽和Na2CO3溶液,用于中和乙酸,溶解乙醇,降低乙酸乙酯在水中的溶解度,故答案為:A;
(3)實驗完畢后,將b試管中的液體充分振蕩,靜置后,溶液分為兩層,乙酸乙酯密度比水小,在上層,常用分液操作將兩層液體分離,故答案為:上層;分液;
(4)設得到的乙酸乙酯的物質的量為x,
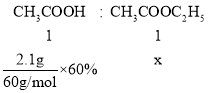
x=0.021mol,m(CH3COOC2H5)=0.021mol×88g/mol≈1.85g,即得到乙酸乙酯的質量為1.85g,故答案為:1.85。


 黃岡經典趣味課堂系列答案
黃岡經典趣味課堂系列答案 啟東小題作業本系列答案
啟東小題作業本系列答案科目:高中化學 來源: 題型:
【題目】某藥物中間體的合成路線如下:
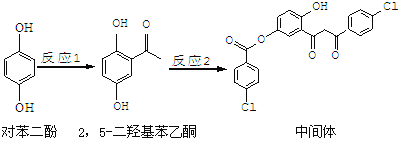
下列說法正確的是
A.對苯二酚和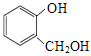 互為同系物
互為同系物
B.1 mol該中間體最多可與7 mol氫氧化鈉反應
C.2,5—二羥基苯乙酮能發生加成、水解等反應
D.該中間體分子含有羰基和羥基兩種含氧官能團
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列離子方程式正確的是( )
A.氫氧化鋇溶液與稀硫酸反應:Ba2++S![]() +H++OH-BaSO4↓+H2O
+H++OH-BaSO4↓+H2O
B.刻制印刷電路板的反應:Fe3++CuFe2++Cu2+
C.氯氣與氫氧化鈉溶液反應:Cl2+2OH-Cl-+ClO-+H2O
D.稀硫酸滴到鐵片上:2Fe+6H+2Fe3++3H2↑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是元素周期表的一部分,除標出的元素外,表中的每個編號代表一種元素。請根據要求回答問題:
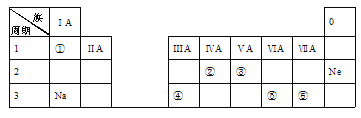
(1)④的原子序數是________;
(2)⑤的原子結構示意圖是____________;
(3)②和③兩種元素的非金屬性強弱關系是:②______③(填“>”、“<”或“=”);
(4)①和⑥兩種元素組成的化合物中含有的化學鍵是_____(填“共價”或“離子”)鍵。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鋁的利用成為人們研究的熱點,是新型電池研發中重要的材料。
(1)通過以下反應制備金屬鋁。
反應I: Al2O3(s)+AlCl3(g)+3C(s)=3AlCl(g)+3CO(g) ΔH1=akJ·mol-1
反應Ⅱ:Al2O3(s)+3C(s) =2Al(g)+3CO(g) ΔH2=bkJ·mol-1
反應Ⅲ:3AlCl(g)=2Al(l)+AlCl3(g) ΔH3
①反應Ⅲ的△H3=____kJ/mol。
②950℃時,鋁土礦(Al2O3)與足量的焦炭和C12反應可制得AlCl3。該反應的化學方程式是 _____________________________
(2)在高溫條件下進行反應:2Al(l)+AlCl3 (g)![]() 3AlCl(g)
3AlCl(g)
①向圖1所示的起始容積相等的兩個密閉容器A、B中加入足量的Al粉,再分別充入1molAICl3 (g),在相同的高溫下進行反應。圖2表示A容器內的AlC13(g)體積分數隨時間的變化圖,在圖2中畫出 B容器內AlCl3 (g)體積分數隨時間的變化曲線____________。
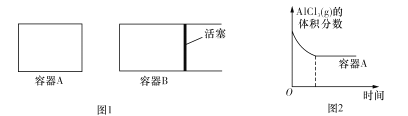
②1 100℃時,向2L密閉容器中通入3mol AlCl(g),發生反應:3AlCl(g)![]() 2Al(l)+AlCl3 (g)。已知該溫度下AlCl(g)的平衡轉化率為80%,則該反應的平衡常數K= ___。在反應達到平衡后,再加入1molAlCl(g),重新達到平衡時AlCl(g)的平衡轉化率將 ___(填“增大”“減小”或“不變”)。
2Al(l)+AlCl3 (g)。已知該溫度下AlCl(g)的平衡轉化率為80%,則該反應的平衡常數K= ___。在反應達到平衡后,再加入1molAlCl(g),重新達到平衡時AlCl(g)的平衡轉化率將 ___(填“增大”“減小”或“不變”)。
③加入3 mol AlCl(g),在不同壓強下發生反應,溫度對產率的影響如圖3所示。則此反應選擇溫度為 _____________________
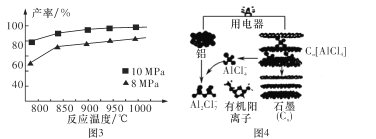
(3)鋁可以用來制作快速放電鋁離子二次電池,該電池以金屬鋁和石墨為電極,用AlCl4-、Al2Cl2-和有機陽離子組成電解質溶液,其工作原理如圖4所示。
①該電池放電時,AlCl4-向 ___(填“鋁電極”或“石墨電極”)方向移動。
②該電池充電時,陰極的電極反應式為____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】由下列實驗現象一定能得出相應結論的是
選項 | A | B | C | D |
裝置或操作 | 取兩支試管各加入4 mL 0.01 mol/L的草酸溶液,分別滴加2 mL 0.1 mol/L、0.2 mol/L的高錳酸鉀溶液 |
|
| 向分別盛有5 mL 0.1 mol/L的硫代硫酸鈉溶液的試管中滴加5 mL 0.1 mo/L的硫酸溶液,一段時間后,分別放在冷水和熱水中。 |
現象 | 褪色并觀察褪色的時間 | 左邊棉球變黃,右邊棉球變藍 | 試管中先出現淡黃色固體,后出現黃色固體 | 試管中液體變渾濁且熱水中首先出現渾濁 |
結論 | 其他條件不變時,反應物濃度越大,反應速率越快 | 氧化性:Cl2>Br2>I2 | 溶解度:AgCl>AgBr>AgI | 不能說明溫度越高,速率越快 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上用氨氣和氫氣直接合成氨,并通過下列轉化過程制備硝酸:
![]()
(1)上述物質中為紅棕色氣體的是____(填化學式);
(2)NH3溶于水所得溶液呈___(填“酸性”、 “堿性”或“中性” );
(3)配平NO2→HNO3的化學方程式:3NO2 +H2O = ___HNO3 + NO。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是元素周期表的一部分,除標出的元素外,表中的每個編號代表一種元素。請根據要求回答問題:
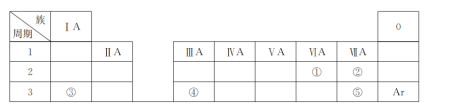
(1)①的元素符號是________;
(2)②和⑤的原子半徑大小關系是②________⑤(填“>”“<”或“=”);
(3)③和⑤形成的化合物含有的化學鍵是__________(填“離子鍵”或“共價鍵”);
(4)③、④的最高價氧化物對應的水化物相互反應的離子方程式為_________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鋰離子電池的正極材料是含鋰的鈷酸鋰(LiCoO2),充電時LiCoO2中Li被氧化,Li+遷移并以原子形式嵌入電池負極材料碳(C6)中,用LiC6表示。電池反應為CoO2+LiC6![]() LiCoO2+C6,下列說法正確的是( )
LiCoO2+C6,下列說法正確的是( )
A.充電時,電池的負極反應為LiC6-e-=Li++C6
B.放電時,電池的正極反應為CoO2+Li++e-=LiCoO2
C.羧酸、醇等含活潑氫的有機物可用作鋰離子電池的電解質
D.鋰離子電池的比能量(單位質量釋放的能量)低
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com