
【題目】電-Fenton法是用于水體中有機污染物降解的高級氧化技術,其反應原理如圖所示。其中電解產生的H2O2與Fe2+發生Fenton反應:H2O2+Fe2+![]() Fe3++OH-+·OH,生成的羥基自由基(·OH)能氧化降解有機污染物。下列說法中正確的是( )
Fe3++OH-+·OH,生成的羥基自由基(·OH)能氧化降解有機污染物。下列說法中正確的是( )
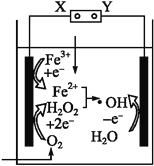
A. 電源的X極為正極,Y極為負極
B. 陰極的電極反應式為Fe2+-e-![]() Fe3+
Fe3+
C. 每消耗1molO2,整個電解池中理論上可產生2mol·OH
D. 陽極的電極反應式為H2O-e-![]() H++·OH
H++·OH
【答案】D
【解析】A、電源的X電極連接的電極上為氧氣得電子生成雙氧水的還原反應,則該電極為陰極,所以A為負極,則Y極為正極,故A錯誤;B、O2、Fe3+在陰極上得電子發生還原反應,反應式為Fe3++e-═Fe2+,O2+2H2O+2e-═H2O2+2OH-,故B錯誤;C、1molO2轉化為2molH2O2轉移2mole-,由Fe2++H2O2=Fe3++OH-+·OH可知,生成2mol·OH,轉移2mole-,在陽極上生成2mol·OH,所以消耗1molO2,可以產生4mol·OH,故C錯誤;D、陽極上水失電子生成羥基和氫離子,其電極方程式為:H2O-e-=·OH+H+,故D正確;故選D。


 沖刺100分1號卷系列答案
沖刺100分1號卷系列答案科目:高中化學 來源: 題型:
【題目】Ⅰ.高鐵酸鉀(K2FeO4)是一種新型、高效、多功能綠色水處理劑,比Cl2、O2、ClO2、KMnO4氧化性更強,無二次污染,工業上是先制得高鐵酸鈉,然后在低溫下,向高鐵酸鈉溶液中加入KOH至飽和,使高鐵酸鉀析出。
(1)干法制備高鐵酸鈉的主要反應為:2FeSO4 + 6 Na2O2 = 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2↑,該反應中還原劑是___________________(填化學式),被2 mol FeSO4還原的過氧化鈉為_________mol
(2)濕法制備高鐵酸鉀(K2FeO4)的反應體系中有六種微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。寫出堿性條件下制高鐵酸鉀的離子反應方程式:__________________________
Ⅱ.已知:2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-。
(1)含有1 mol FeI2和2 mol FeBr2的溶液中通入2 mol Cl2,此時被氧化的離子是____________,被氧化的離子的物質的量分別是_____________________________________________
(2)若向含a mol FeI2和b mol FeBr2的溶液中通入c mol Cl2,當I-、Fe2+被氧化時,c為_____________(用含a、b的代數式表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于電解質的敘述正確的是( )
A.導電性很強的物質
B.在溶于水或熔融狀態下能導電的化合物
C.在溶于水和熔融狀態下均電離的化合物
D.可溶性鹽類
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖是中學化學中常用于混合物的分離和提純的裝置,請根據裝置回答有關問題:
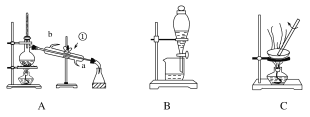
(1)裝置A中玻璃儀器①的名稱是________,進水的方向是從____口(填字母)進水。
(2)利用裝置B分液時為使液體順利滴下,應進行的具體操作是_________________。
(3)從氯化鉀溶液中得到氯化鉀固體,應選擇裝置________(填字母,下同);從碘水中分離出I2,應選擇裝置________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】日常生活中的許多現象與化學反應有關,下列現象與氧化還原反應無關的是 ( )
A. 銅鑄塑像上出現銅綠[Cu2(OH)2CO3] B. 充有氫氣的氣球遇明火爆炸
C. 大理石雕像被酸雨腐蝕毀壞 D. 鐵質菜刀生銹
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組溶液中的各種溶質的物質的量濃度均為0.1 mol/L。①H2S溶液;②KHS溶液;③K2S溶液;④H2S和KHS混合溶液。 下列說法正確的是
A. 溶液pH從大到小的順序是:③ > ② > ① > ④
B. 在KHS溶液中有:c(H+) + c(K+) = c(OH-) + c(HS-) + c(S2-)
C. c(H2S)從大到小的順序是:① > ④ > ③ > ②
D. 在H2S和KHS混合溶液中有:c(H2S) + c(HS-) + c(S2-) = 2c(K+)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知電極上每通過96500 C的電量就會有1 mol電子發生轉移。精確測量金屬離子在惰性電極上以鍍層形式沉積的金屬質量,可以確定電解過程中通過電解池的電量。實際測量中,常用銀電量計,如圖所示。下列說法不正確的是

A. 若要測定電解飽和食鹽水時通過的電量,可將該銀電量計中的銀棒與待測電解池的陽極相連,鉑坩堝與電源的負極相連。
B. 稱量電解前后鉑坩堝的質量變化,得金屬銀的沉積量為108.0 mg,則電解過程中通過電解池的電量為96.5 C
C. 實驗中,為了避免銀溶解過程中可能產生的金屬顆粒掉進鉑坩堝而導致測量誤差,常在銀電極附近增加一個收集網袋。若沒有收集網袋,測量結果會偏高。
D. 電量計中的銀棒應與電源的正極相連,鉑坩堝上生的電極反應是:Ag+ + e- = Ag
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下,在恒容密閉容器中,能表示反應X(g)+2Y(g) ![]() 2Z(g)一定達到化學平衡狀態的是( )
2Z(g)一定達到化學平衡狀態的是( )
①X、Y、Z的物質的量之比為1∶2∶2
②X、Y、Z的濃度不再發生變化
③容器中的壓強不再發生變化
④單位時間內生成n mol Z,同時生成2n mol Y
A. ①② B. ①④ C. ②③ D. ③④
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com