
【題目】鐵及其化合物在生產(chǎn)、生活中有廣泛的應(yīng)用。
(1)復(fù)合氧化物鐵酸錳(MnFe2O4)可用于熱化學循環(huán)分解制氫氣,原理如下:
①MnFe2O4(s)===MnFe2O(4-x)(s)+x/2O2(g) ΔH1
②MnFe2O(4-x)(s)+xH2O(g)===MnFe2O4(s)+xH2(g) ΔH2
③2H2O(g)===2H2(g)+O2(g) ΔH3
則:ΔH3與ΔH1、ΔH2的關(guān)系為ΔH3=________。
(2)納米鐵是重要的儲氫材料,可用下列反應(yīng)制得:Fe(s)+5COFe(CO)5(g) ΔH<0。在1 L恒容密閉容器中加入足量鐵粉和0.5 mol CO,在T1、T2不同溫度下進行反應(yīng),測得c(CO)與溫度、時間的關(guān)系如圖1所示。

①T1________(填“>”或“<”)T2。
②T2溫度下,上述反應(yīng)的平衡常數(shù)K=________(結(jié)果不要求帶單位)。
(3)高鐵酸鉀(K2FeO4)被人們稱為“綠色化學”凈水劑。高鐵酸鉀在酸性至弱堿性條件下不穩(wěn)定。
①工業(yè)上用KClO與Fe(NO3)3溶液反應(yīng)制得K2FeO4,反應(yīng)的離子方程式為____________________。制備K2FeO4時,KClO飽和溶液與Fe(NO3)3飽和溶液混合的操作為________________________。
②已知K2FeO4在水解過程中鐵元素形成的微粒分布分數(shù)與pH的關(guān)系如圖所示。


向pH=6的溶液中加入KOH溶液,發(fā)生反應(yīng)的離子方程式為____________________________________。
(4)電解法可制得K2FeO4,裝置如圖所示。陽極的電極反應(yīng)式為________。
【答案】2(ΔH1+ΔH2)/x > 8×103 3ClO-+2Fe3++10OH-===2FeO42-+3Cl-+5H2O 在攪拌下,將Fe(NO3)3飽和溶液緩慢滴加到KClO飽和溶液中 HFeO4-+OH-===FeO42-+H2O Fe-6e-+8OH-===FeO42-+4H2O
【解析】
(1)根據(jù)蓋斯定律結(jié)合熱化學方程式計算可得ΔH3與ΔH1、ΔH2的關(guān)系;
(2) ①該反應(yīng)的正反應(yīng)為放熱反應(yīng),升高溫度平衡向逆反應(yīng)方向移動,CO的濃度增大,以此判斷;
②根據(jù)圖中數(shù)據(jù),列出三段式,找出平衡濃度,根據(jù)K=![]() 計算;
計算;
(3)①ClO-與Fe3+反應(yīng)生成FeO42-,ClO-被還原為Cl-,根據(jù)得失電子守恒和電荷守恒及原子守恒寫出反應(yīng)的離子方程式;
制備K2FeO4時,K2FeO4在Fe3+和Fe(OH)3催化作用下發(fā)生分解,應(yīng)把Fe(NO3)3飽和溶液滴加到KClO溶液中;
②由圖可知,pH=6時溶液主要存在HFeO4-,加入KOH溶液發(fā)生中和,以此寫出該反應(yīng)的離子方程式;
(4)鐵是陽極失去6個電子生成FeO42-,據(jù)此書寫陽極反應(yīng)式。
(1) 已知:①MnFe2O4(s)===MnFe2O(4-x)(s)+x/2O2(g) ΔH1
②MnFe2O(4-x)(s)+xH2O(g)===MnFe2O4(s)+xH2(g) ΔH2
③2H2O(g)===2H2(g)+O2(g) ΔH3
由熱化學方程式結(jié)合蓋斯定律,將反應(yīng)①![]() 2+②
2+②![]() 2可得2xH2O(g)===2xH2(g)+xO2(g) ΔH=
2可得2xH2O(g)===2xH2(g)+xO2(g) ΔH=
2(ΔH1+ΔH2),反應(yīng)③![]() x可以得到相同的熱化學方程式,則有ΔH3=2(ΔH1+ΔH2)/x。
x可以得到相同的熱化學方程式,則有ΔH3=2(ΔH1+ΔH2)/x。
故答案為:2(ΔH1+ΔH2)/x;
(2) ①該反應(yīng)的正反應(yīng)為放熱反應(yīng),升高溫度平衡向逆反應(yīng)方向移動,平衡時CO的濃度增大,由圖可知,T2時CO平衡濃度小于T1時,則T1>T2。
②T2溫度下,
Fe(s)+5CO![]() Fe(CO)5(g)
Fe(CO)5(g)
起始(mol/L) 0.5 0
轉(zhuǎn)化(mol/L) 0.4 0.08
平衡(mol/L) 0.1 0.08
平衡常數(shù)K=![]() =
=![]() =8×103,
=8×103,
故答案為:> ;8×103;
(3)①ClO-與Fe3+反應(yīng)生成FeO42-,ClO-被還原為Cl-,根據(jù)得失電子守恒和電荷守恒及原子守恒可得反應(yīng)的離子方程式為3ClO-+2Fe3++10OH-===2FeO42-+3Cl-+5H2O;
制備K2FeO4時,K2FeO4在Fe3+和Fe(OH)3催化作用下發(fā)生分解,應(yīng)把Fe(NO3)3飽和溶液滴加到KClO溶液中,具體操作為:在攪拌下,將Fe(NO3)3飽和溶液緩慢滴加到KClO飽和溶液中;
故答案為:3ClO-+2Fe3++10OH-===2FeO42-+3Cl-+5H2O;在攪拌下,將Fe(NO3)3飽和溶液緩慢滴加到KClO飽和溶液中;
②由圖可知,pH=6時溶液主要存在HFeO4-,加入KOH溶液發(fā)生中和,反應(yīng)的離子方程式為HFeO4-+OH-===FeO42-+H2O,
故答案為:HFeO4-+OH-===FeO42-+H2O;
(4)鐵是陽極失去6個電子,因此陽極電極反應(yīng)式為Fe-6e-+8OH-=FeO42-+4H2O,
故答案為:Fe-6e-+8OH-===FeO42-+4H2O。


科目:高中化學 來源: 題型:
【題目】下列是典型晶體的結(jié)構(gòu)示意圖,從①到⑥對應(yīng)正確的是:
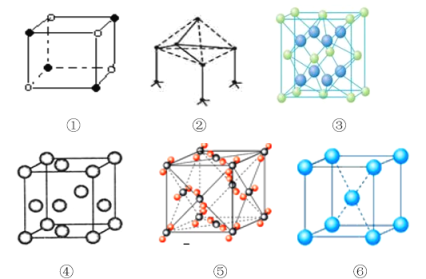
選項 | ① | ② | ③ | ④ | ⑤ | ⑥ |
A | NaCl | 單質(zhì)硅 | CaF2 | Au | CO2 | K |
B | CaF2 | SiC | 金剛石 | Cu | CO2 | CsCl |
C | CsCl | 金剛石 | CaF2 | Cu | CO2 | Mg |
D | NaCl | BN | Au | CaF2 | CO2 | Na |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1).對于下列反應(yīng):2SO2 + O2 ![]() 2SO3 , 如果2min內(nèi)SO2的濃度由6 mol/L下降為2 mol/L,那么,用SO2濃度變化來表示的化學反應(yīng)速率為__________,用O2濃度變化來表示的反應(yīng)速率為__________。
2SO3 , 如果2min內(nèi)SO2的濃度由6 mol/L下降為2 mol/L,那么,用SO2濃度變化來表示的化學反應(yīng)速率為__________,用O2濃度變化來表示的反應(yīng)速率為__________。
(2)反應(yīng)N2+3H2![]() 2NH3 ΔH<0 ,達平衡后,不同時刻改變外界條件時正逆反應(yīng)速率變化如圖,請判斷某時刻所改變的條件。
2NH3 ΔH<0 ,達平衡后,不同時刻改變外界條件時正逆反應(yīng)速率變化如圖,請判斷某時刻所改變的條件。

可能改變的外界條件:t1__________,t2__________ ,t3__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Y是合成香料、醫(yī)藥、農(nóng)藥及染料的重要中間體,可由X在酸性條件下反應(yīng)得到:

下列說法正確的是( )
A. X分子中所有碳原子可能共平面
B. X、Y分別與足量H2加成后的分子中均含有手性碳原子
C. Y可以發(fā)生顯色、氧化和還原反應(yīng),還可以與甲醛發(fā)生縮聚反應(yīng)
D. 等物質(zhì)的量的X、Y分別與NaOH溶液反應(yīng),最多消耗NaOH的物質(zhì)的量之比為4∶3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】醋酸和一水合氨是中學化學中常見的弱電解質(zhì)。
(1)常溫下,某研究性學習小組設(shè)計了如下方案證明醋酸為弱電解質(zhì),你認為方案可行的是_______(填序號)
①配制一定量的0.10 mol/L CH3COOH溶液,然后測溶液的pH,若pH大于1,則證明醋酸為弱電解質(zhì)。
②用醋酸溶液和鹽酸做導(dǎo)電性實驗,若醋酸溶液導(dǎo)電性弱,則證明醋酸為弱電解質(zhì)。
③將pH=2的CH3COOH溶液加水稀釋100倍后,若pH>4,則證明醋酸為弱電解質(zhì)。
④配制一定量的CH3COONa溶液,測其pH,若pH大于7,則證明醋酸為弱電解質(zhì)。
(2)若25℃時,0.10 mol/L的CH3COOH的電離度為1%,則該溶液的pH=________,由醋酸電離出的c(H+)約為水電離出的c(H+)的_________倍。
(3)已知在25℃時,醋酸的電離平衡常數(shù)為Ka=1.8×10-5。常溫下,0.1mol/LNaOH溶液V1 mL和0.2mol/LCH3COOH溶液V2 mL混合后(忽略混合前后溶液體積的變化)溶液的pH=7。
①反應(yīng)后溶液中離子濃度的大小關(guān)系為_________________________________________________。
②V1:V2 __________(填“>”、“<”或“=”)2:1
③c(CH3COO-):c(CH3COOH)=__________________。
(4)常溫下,可用氨水吸收廢氣中的CO2得到NH4HCO3溶液,在該溶液中,c(NH4+)_______(填“>”、“<”或“=”)c(HCO3-);反應(yīng)NH4++HCO3-+H2O![]() NH3·H2O+H2CO3的平衡常數(shù)K=_________。(已知常溫下NH3·H2O的電離平衡常數(shù)Kb=2×10-5,H2CO3的電離平衡常數(shù)Ka1=4×10-7,Ka2=4×10-11)
NH3·H2O+H2CO3的平衡常數(shù)K=_________。(已知常溫下NH3·H2O的電離平衡常數(shù)Kb=2×10-5,H2CO3的電離平衡常數(shù)Ka1=4×10-7,Ka2=4×10-11)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學通過如下流程制備氧化亞銅:

已知CuCl難溶于水和稀硫酸:Cu2O+2H+==Cu2++Cu+H2O
下列說法不正確的是
A. 步驟②SO2可用Na2SO3替換
B. 步驟③中為防止CuCl被氧化,可用SO2水溶液洗滌
C. 步驟④發(fā)生反應(yīng)的離子方程式為2CuCl+2OH-=Cu2O+2Cl-+H2O
D. 如果Cu2O試樣中混有CuCl和CuO雜質(zhì),用足量稀硫酸與Cu2O試樣充分反應(yīng),根據(jù)反應(yīng)前、后固體質(zhì)量可計算試樣純度
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應(yīng)中屬于氧化還原反應(yīng)的是
A.CuSO4+H2S=CuS↓+H2SO4B.2FeCl3+Cu=2FeCl2+CuCl2
C.Cu2(OH)2CO3![]() 2CuO+CO2↑+H2OD.FeCl3+3NaOH=Fe(OH)3↓+3NaCl
2CuO+CO2↑+H2OD.FeCl3+3NaOH=Fe(OH)3↓+3NaCl
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】砷和鎳均為重要的無機材料,在化工領(lǐng)域具有廣泛的應(yīng)用。
(1)基態(tài)As原子的價層電子的電子云輪廓圖形狀為_____________。與砷同周期的主族元素的基態(tài)原子中,第一電離能最大的為_____________(填元素符號。)
(2)Na3AsO3可用于碘的微量分析。
①Na+的焰色反應(yīng)呈黃色,金屬元素能產(chǎn)生焰色反應(yīng)的微觀原因為__________________________。
②Na3AsO3中所含陰離子的立體構(gòu)型為_____________,寫出一種與其互為等電子體的分子:_____________(填化學式)。
(3) 可用于合成Ni2+的配體,M中C原子的雜化方式為___________,其所含
可用于合成Ni2+的配體,M中C原子的雜化方式為___________,其所含![]() 鍵和π鍵的數(shù)目之比為___________。
鍵和π鍵的數(shù)目之比為___________。
(4)Ni與Ca處于同一周期,且核外最外層電子構(gòu)型相同,但金屬Ni的熔點和沸點均比金屬Ca的高,其原因為___________。區(qū)分晶體Ni和非晶體Ni的最可靠的科學方法為___________。
(5)某砷鎳合金的晶胞結(jié)構(gòu)如下圖所示,設(shè)阿伏加德羅常數(shù)的值為NA,則該晶體的密度ρ=___________g·cm-3。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對可逆反應(yīng)4NH3(g)+ 5O2(g)![]() 4NO(g)+ 6H2O(g),下列敘述正確的是
4NO(g)+ 6H2O(g),下列敘述正確的是
A. 達到化學平衡時,4υ正(O2)= 5υ逆(NO)
B. 若單位時間內(nèi)生成x mol NO的同時,消耗x mol NH3 ,則反應(yīng)達到平衡狀態(tài)
C. 達到化學平衡時,若增加容器體積,則正反應(yīng)速率減少,逆反應(yīng)速率增大
D. 化學反應(yīng)速率關(guān)系是:2υ正(NH3)= 3υ正(H2O)
查看答案和解析>>
國際學校優(yōu)選 - 練習冊列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com