
【題目】甲苯是有機化工生產的基本原料之一。利用乙醇和甲苯為原料,可按下列路線合成分子式均為C9H10O2的有機化工產品E和J。
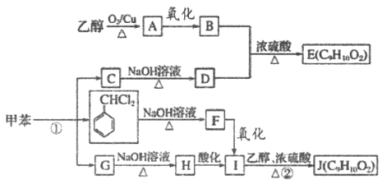
已知以下信息:
①通常在同一個碳原子上連有兩個羥基不穩定,易脫水。
②G的核磁共振氫譜表明其只有三種不同化學環境的氫。
請回答下列問題:
(1)用甲苯制備TNT的反應方程式:_____________。
(2)D的名稱是_____________。
(3)寫出B+D→E的反應方程式:_____________,
(4)①的反應條件為_____________。
(5)F的結構簡式為_____________。
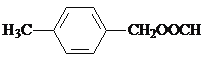
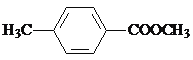
(6)E、J有多種同分異構體,寫出符合下列條件的2種同分異構體的結構簡式_____________、_____________。
①與E、J屬同類物質
②苯環上有兩個取代基
③核磁共振氫譜表明苯環上只有兩組峰
【答案】![]() +3HNO3
+3HNO3![]()
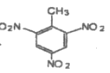 +3H2O 苯甲醇
+3H2O 苯甲醇  光照
光照 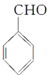
 、
、
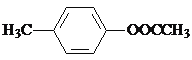 、
、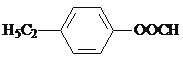 (任選兩種)
(任選兩種)
【解析】
由題中合成路線信息可知,乙醇經催化氧化得到A,所以A是乙醛,A經氧化得到B,所以B是醋酸。在光照條件下甲苯與氯氣發生取代反應生成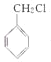 、
、![]() 和
和![]() ,然后在加熱條件下與NaOH溶液發生水解生成對應醇
,然后在加熱條件下與NaOH溶液發生水解生成對應醇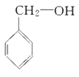 、
、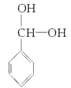 和
和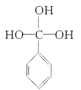 ,由
,由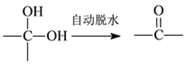 可知,
可知, 會自動脫水轉化為
會自動脫水轉化為 ,
, 會自動脫水、再經酸化轉化為
會自動脫水、再經酸化轉化為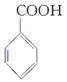 ,
, 也可以氧化為
也可以氧化為 ,與題中信息相符,所以C為
,與題中信息相符,所以C為 、D為
、D為 、F為
、F為 、I為
、I為 ,I與乙醇發生酯化反應生成J,則J為苯甲酸乙酯,結構為
,I與乙醇發生酯化反應生成J,則J為苯甲酸乙酯,結構為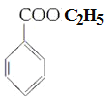 。E和J是同分異構體,所以E是乙酸苯甲酯,結構簡式為
。E和J是同分異構體,所以E是乙酸苯甲酯,結構簡式為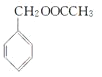 。
。
(1)根據上述分析可知,用甲苯與濃硝酸發生取代反應制備TNT,其反應方程式為:![]() +3HNO3
+3HNO3![]()
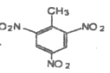 +3H2O;
+3H2O;
(2)D為 ,其名稱是為苯甲醇;
,其名稱是為苯甲醇;
(3)B+D→E是酸與醇發生酯化反應生成酯和水的過程,其化學方程式式為: ;
;
(4)①發生取代反應,其反應條件為光照;
(5)F的結構簡式為 ;
;
(6)①與E、J屬同類物質,則要求分子中有苯環、酯基;②苯環上有兩個取代基且苯環上的一氯代物只有兩種,則兩取代基應置于苯環對位。符合這兩個條件的4種同分異構體結構簡式分別為: 、
、 、
、 、
、 (任選兩種)。
(任選兩種)。


科目:高中化學 來源: 題型:
【題目】根據下列實驗操作和現象得出的結論正確的是
操作 | 現象 | 結論 | |
A | 將 | 溴水和酸性高錳酸鉀溶液均褪色 |
|
B | 向 | 先產生白色沉淀,后產生紅褐色沉淀 |
|
C | 向滴有酚酞的 | 有白色沉淀生成,溶液紅色變淺 |
|
D | 將 | 產生白色沉淀 | 酸性: |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)2017年中科院某研究團隊通過設計一種新型Na-Fe3O4/HZSM-5多功能復合催化劑,成功實現了CO2直接加氫制取辛烷值汽油,該研究成果被評價為“CO2催化轉化領域的突破性進展”。
已知:H2(g)+1/2O2(g)=H2O(l) ΔH1 = -aKJ/mol
C8H18(1)+25/2O2(g)=8CO2(g)+9H2O(1) ΔH2= -bKJ/mol
試寫出25℃、101kPa條件下,CO2與H2反應生成汽油(以C8H18表示)的熱化學方程式_________________________________。
(2)利用CO2及H2為原料,在合適的催化劑(如Cu/ZnO催化劑)作用下,也可合成CH3OH,涉及的反應有:
甲:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H= — 53.7kJ·mol-1 平衡常數K1
CH3OH(g)+H2O(g) △H= — 53.7kJ·mol-1 平衡常數K1
乙:CO2(g)+H2(g) ![]() CO(g)+H2O(g) △H= + 41.2kJ·mol-1 平衡常數K2
CO(g)+H2O(g) △H= + 41.2kJ·mol-1 平衡常數K2
①CO(g)+2H2(g) ![]() CH3OH(g)的平衡常數K=______(用含K1、K2的表達式表示),該反應△H_____0(填“大于”或“小于”)。
CH3OH(g)的平衡常數K=______(用含K1、K2的表達式表示),該反應△H_____0(填“大于”或“小于”)。
②提高CO2轉化為CH3OH平衡轉化率的措施有___________(填寫兩項)。
③催化劑和反應體系的關系就像鎖和鑰匙的關系一樣,具有高度的選擇性。下列四組實驗,控制CO2和H2初始投料比均為1:2.2,經過相同反應時間(t1min)。
溫度(K) | 催化劑 | CO2轉化率(%) | 甲醇選擇性(%) | 綜合選項 |
543 | Cu/ZnO納米棒材料 | 12.3 | 42.3 | A |
543 | Cu/ZnO納米片材料 | 11.9 | 72.7 | B |
553 | Cu/ZnO納米棒材料 | 15.3 | 39.1 | C |
553 | Cu/ZnO納米片材料 | 12.0 | 70.6 | D |
由表格中的數據可知,相同溫度下不同的催化劑對CO2的轉化為CH3OH的選擇性有顯著影響,根據上表所給數據結合反應原理,所得最優選項為___________(填字母符號)。
(3)以CO、H2為原料合成甲醇的反應為:CO(g)+2H2(g)![]() CH3OH(g)。在體積均為2L的三個恒容密閉容器Ⅰ、Ⅱ、Ⅲ中,分別都充入1molCO和2molH2,三個容器的反應溫度分別為T1、T2、T3且恒定不變。下圖為三個容器中的反應均進行到5min時H2的體積分數示意圖,其中有一個容器反應一定達到平衡狀態。
CH3OH(g)。在體積均為2L的三個恒容密閉容器Ⅰ、Ⅱ、Ⅲ中,分別都充入1molCO和2molH2,三個容器的反應溫度分別為T1、T2、T3且恒定不變。下圖為三個容器中的反應均進行到5min時H2的體積分數示意圖,其中有一個容器反應一定達到平衡狀態。
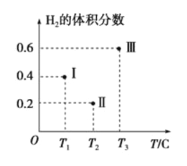
①0~5min時間內容器Ⅱ中用CH3OH表示的化學反應速率為_________________。
②三個容器中一定達到平衡狀態的是容器________(填寫容器代號)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】綠色化學對化學反應提出了“原子經濟性”(原子節約)的新概念及要求。理想的原子經濟性反應是原料分子中的全部轉變成所需產物,不產生副產物,實現零排放。以下反應中符合綠色化學原理的是
A. 乙烯與O2在銀催化下生成環氧乙烷![]()
B. 乙烷與氯氣制備氯乙烷
C. 苯和乙醇為原料,在一定條件下生產乙苯
D. 乙醇和濃硫酸共熱制備乙烯
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】D-58和NM-3是臨床試用的小分子抗癌藥物,結構如下:
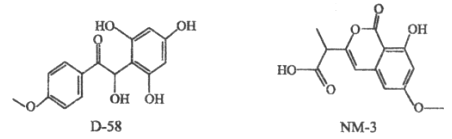
下列說法中不正確的是
A. D-58遇FeCl3溶液顯紫色
B. NM-3能與Br2發生取代和加成反應
C. 兩者都不能發生消去反應
D. 兩者能與NaHCO3溶液反應放出氣體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學課外活動小組以海帶為原料獲得少量碘水,并以四氯化碳(沸點76.80C)為溶劑將碘從碘水中提取出來,具體過程如圖所示。

請回答下列問題:
(1)操作①的名稱為________________、_________________;
(2)向含碘單質的水溶液中加入CCl4振蕩、靜置后,觀察到的現象是______________________;
(3)操作③中,將含碘單質的水溶液與CCl4在分液漏斗中混合、振蕩搖勻放在鐵架臺的鐵圈上,分液漏斗的下端尖嘴處緊貼在承接的燒杯內壁上靜置后,下面的操作步驟是_______________________。
(4)從含碘的有機溶劑中經過蒸餾可以提取碘和回收有機溶劑,該實驗需要的主要玻璃儀器除酒精燈、燒杯、溫度計、錐形瓶、牛角管外,還需要____________________,實驗中溫度計水銀球所處位置為___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學反應原理對化學反應的研究具有指導意義。
(1)機動車廢氣排放已成為城市大氣污染的重要來源。氣缸中生成NO的反應為:N2(g)+O2(g) ![]() 2NO(g) △H >0。汽車啟動后,氣缸內溫度越高,單位時間內NO排放量越大,請分析兩點可能的原因___________、_____________。
2NO(g) △H >0。汽車啟動后,氣缸內溫度越高,單位時間內NO排放量越大,請分析兩點可能的原因___________、_____________。
(2)由金紅石TiO2制取單質Ti,涉及到的步驟為:
TiO2![]() TiCl4
TiCl4![]() Ti
Ti
已知:①Cs+O2g=CO2g; H=3935 kJ·mol1
②2COg+O2g=2CO2g; H=566 kJ·mol1
③TiO2s+2Cl2g=TiCl4s+O2g; H=+141 kJ·mol1
則TiO2s+2Cl2g+2Cs=TiCl4s+2COg的H=________________。
(3)氯氣在298K、100kPa時,在1L水中可溶解0.09mol,實驗測得溶于水的Cl2約有1/3與水反應。該反應的化學方程式為______,在上述平衡體系中加入少量NaOH固體,溶液中Cl—濃度_______(選填“增大”、“減小”或“不變”)。
(4)一定條件下,Fe3+和I—在水溶液中的反應是2I—+2Fe3+![]() I2+2Fe2+,當反應達到平衡后,加入CCl4充分振蕩,且溫度不變,上述平衡向_______(選填“正反應”或“逆反應”)方向移動。請設計一種使該反應的化學平衡逆向移動的實驗方案_____。
I2+2Fe2+,當反應達到平衡后,加入CCl4充分振蕩,且溫度不變,上述平衡向_______(選填“正反應”或“逆反應”)方向移動。請設計一種使該反應的化學平衡逆向移動的實驗方案_____。
(5)用Cl2生產某些含氯有機物時會產生副產物HCl。利用反應A,可實現氯的循環利用。反應A:4HCl+O2![]() 2Cl2+2H2O
2Cl2+2H2O
已知:ⅰ.此條件下反應A中,4 mol HCl被氧化,放出115.6 kJ的熱量。
ⅰⅰ.![]()
![]()
①寫出此條件下,反應A的熱化學方程式___________。
②斷開1 mol H—O鍵與斷開1 mol H—Cl鍵所需能量相差約為__________kJ。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據乙烯、乙酸、乙醇的性質類比,有機物的結構簡式如圖,該物質的化學性質中說法正確的有:

①能加聚也能縮聚;②1mol該有機物分別可跟1 molBr2、4molH2加成;③可使酸性KMnO4溶液褪色;④可跟Na2CO3溶液反應;⑤1mol該有機物可消耗2 mol NaOH;⑥可在堿性條件下水解
A.2個B.3個C.4個D.5個
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com