
【題目】一種離子晶體的晶胞如圖所示。其中陽離子A以![]() 表示,陰離子B以
表示,陰離子B以![]() 表示。關于該離子晶體的說法正確的是( )
表示。關于該離子晶體的說法正確的是( )
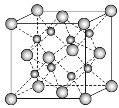
A. 陽離子的配位數為8,化學式為AB
B. 陰離子的配位數為4,化學式為A2B
C. 每個晶胞中含4個A
D. 每個A周圍有4個與它等距且最近的A
 中考利劍中考試卷匯編系列答案
中考利劍中考試卷匯編系列答案 教育世家狀元卷系列答案
教育世家狀元卷系列答案 黃岡課堂作業本系列答案
黃岡課堂作業本系列答案 單元加期末復習先鋒大考卷系列答案
單元加期末復習先鋒大考卷系列答案科目:高中化學 來源: 題型:
【題目】氮化鉻(CrN)是一種良好的耐磨材料,實驗室可用無水氯化鉻(CrCl3)與氨氣在高溫下反應制備,反應原理為CrCl3+NH3![]() CrN+3HCl.回答下列問題:
CrN+3HCl.回答下列問題:
(1)制備無水氯化鉻。氯化鉻有很強的吸水性,通常以氯化鉻晶體(CrCl3·6H2O)的形式存在。直接加熱脫水往往得到Cr2O3,有關反應的化學方程式為______________,以氯化鉻晶體制備無水氯化鉻的方法是_____________________________。
(2)制備氮化鉻。某實驗小組設計制備氮化鉻的裝置如下圖所示(夾持與加熱裝置省略):
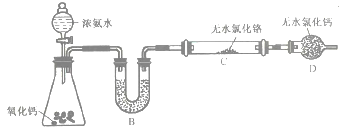
①裝置A中發生反應的化學方程式為_____________________。
②實驗開始時,要先打開裝置A中活塞,后加熱裝置C,目的是___________________。
③裝置B中盛放的試劑是____________,裝置D的作用是_____________________。
④有同學認為該裝置有一個缺陷,該缺陷是_______________________。
(3)氯化鉻的純度測定。制得的CrN中含有Cr2N雜質,取樣品14.38g在空氣中充分加熱,得固體殘渣(Cr2O3)的質量為16.72g,則樣品中CrN的質量分數為_____________(結果保留3位有效數字)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上將苯的蒸汽通過赤熱的鐵合成一種可作傳熱載體的化合物,該化合物分子中苯環上的一氯化物有3種,1mol該化合物催化加氫時最多消耗6mol氫氣,判斷這種化合物可能是(提示:在一定條件下,醛基也可以與H2發生加成反應)( )
A. ![]() B.
B. ![]()
C. ![]() D.
D. 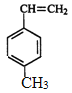
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】銅單質及其化合物在很多領域有重要的用途,如金屬銅用來制造電線電纜,五水硫酸銅可用作殺菌劑。
(1)Cu位于元素周期表第IB族。Cu2+的核外電子排布式為____________。
(2)下圖是銅的某種氧化物的晶胞結構示意圖,可確定該晶胞中陰離子的個數為___________。
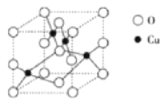
(3)往硫酸銅溶液中加入過量氨水,可生成[Cu(NH3)4]2+配離子。已知NF3與NH3的空間結構都是三角錐形,但NF3不易與Cu2-形成配離子,其原因是__________。
(4)Cu2O的熔點比Cu2S的________(填“高”或“低”)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA表示阿伏加德羅常數的值,下列說法中正確的個數是( )
①過氧化鈉與水反應時,生成0.1mol氧氣轉移的電子數為0.2NA
②5NH4NO3![]() 2HNO3+4N2↑+9H2O反應中,生成28g N2時,轉移的電子數目為3.75NA
2HNO3+4N2↑+9H2O反應中,生成28g N2時,轉移的電子數目為3.75NA
③Na2O2投入到紫色石蕊試液中,溶液先變藍,后褪色;
④3mol單質鐵完全轉化為Fe3O4,失去8NA個電子
⑤標準狀態下,2.24L CH3CH2OH中質子數為3.4NA
⑥將100mL 0.1mol/L的FeCl3溶液滴入沸水中可制得Fe(OH)3膠粒0.01NA
⑦區別NaHCO3與Na2CO3溶液,可用Ca(OH)2溶液
A.3B.4C.5D.6
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是( )
A. 有機物(![]() )的名稱為2-甲基-1-丙醇
)的名稱為2-甲基-1-丙醇
B. 芥子醇( )能發生氧化、取代、水解、加聚反應
)能發生氧化、取代、水解、加聚反應
C. 1mol綠原酸( )與足量溴水反應,最多消耗4molBr2
)與足量溴水反應,最多消耗4molBr2
D. 有機物(俗稱“一滴香”)( )的一種含苯環的同分異構體能發生銀鏡反應
)的一種含苯環的同分異構體能發生銀鏡反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)選擇下列實驗方法分離物質,將分離方法的序號填在橫線上。
A 萃取分液 B 升華 C 結晶 D 過濾 E 蒸餾 F 分液
①分離飽和食鹽水與沙子的混合物______;
②從硝酸鉀和氯化鈉的混合液中獲得硝酸鉀______;
③從碘水中提取碘單質______;
④分離水和汽油的混合物______;
⑤分離![]() 沸點為
沸點為![]() 和甲苯
和甲苯![]() 沸點為
沸點為![]() 的混合物______。
的混合物______。
(2)0.4 mol某氣體的體積為9.8L,則該氣體的氣體摩爾體積為_____。
(3)標準狀況下,測得1.92克某氣體的體積為672mL,則此氣體的相對分子質量為___。
(4)實驗室用Na2CO3·10H2O晶體配制0. 5mol/L的Na2CO3溶液970mL,應用托盤天平稱取Na2CO3·10H2O的質量是____。
(5)已知兩種堿AOH和BOH的摩爾質量之比為5:7,現將7mol AOH與5mol BOH混合后,從中取出5.6g,恰好可以中和100ml濃度為1.2mol/L的鹽酸,則AOH的摩爾質量為_____。
(6)某學生欲用12mol·L-1濃鹽酸和蒸餾水配制500 mL 0.3 mol·L-1的稀鹽酸。
①該學生需要用量筒量取____mL上述濃鹽酸進行配制。
②下列實驗操作會導致所配制的稀鹽酸的物質的量濃度偏小的是____(填序號)。
a 用量筒量取濃鹽酸時俯視觀察凹液面
b 將量取濃鹽酸的量筒進行洗滌,并將洗滌液轉移到容量瓶中
c 稀釋濃鹽酸時,未冷卻到室溫即轉移到容量瓶中
d 定容后經振蕩、搖勻、靜置,發現液面下降,再加適量的蒸餾水
e 容量瓶洗滌干凈后未干燥
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氟苯水楊酸(diflunisal)是一種新型的水楊酸類消炎解熱鎮痛良藥,具有強效、長效低毒等特點。一種可行的合成路線如下(催化劑及溶劑等已省去):
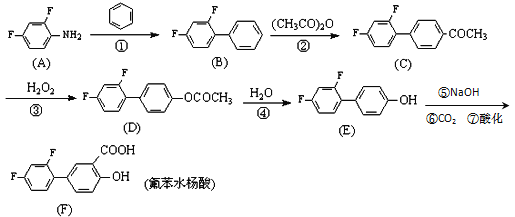
試回答下列問題:
(1)有關氟苯水楊酸的下列說法正確的是______________(選填序號)。
A 分子中只含兩種官能團
B 分子中所有原子可以處于同一平面(已知:HCOOH所有原子可在同一平面)
C 1mol氟苯水楊酸與足量的碳酸氫鈉溶液反應,可生成2molCO2
D 在一定pH條件下,氟苯水楊酸遇FeCl3溶液能發生顯色反應
E 在一定條件下,氟苯水楊酸能發生取代反應
(2)圖中有機物(A)為2,4-二氟苯胺,它的化學式為_______。A的同分異構體中,含有苯環且與A具有相同官能團的同分異構體有_____種(不包括A)。
(3)上述①②③④反應中屬于取代反應的有:_________。
(4)反應②的方程式為:____________________________。(不需注明反應條件)
(5)反應③有2種生成物,另一種生成物是無機物,其化學式為______
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】英國科學家希爾發現,離體的葉綠體懸浮液中加入適當的電子受體(如草酸鐵),在光照時可使水分解而釋放氧氣,從而證明了氧的釋放與CO2還原是不同的過程,將對光合作用的研究上升到細胞層面。該反應方程式為4Fe3++2H2O![]() 4Fe2++4H++O2↑,下列有關希爾反應說法錯誤的是( )
4Fe2++4H++O2↑,下列有關希爾反應說法錯誤的是( )
A. 水在光反應中起供氫體和電子供體雙重作用
B. 反應后溶液pH減小
C. 生成標準狀況下11.2 L O2時,Fe3+得電子數為2NA
D. 葉綠體本身被氧化
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com