
【題目】下列解釋實驗事實的方程式正確的是
A.用氫氧化鈉溶液去除鋁條表面的氧化膜:Al2O3+2OH—=2AlO2—+H2O
B.銅片溶于稀硝酸產生無色氣體:Cu+4H++2NO3—=Cu2++2NO2↑+2H2O
C.氫氧化亞鐵在空氣中變質:2Fe(OH)2+O2+2H2O=2Fe(OH)3
D.碳酸鈉溶液呈堿性:CO32—+2H2O![]() H2CO3+2OH—
H2CO3+2OH—
科目:高中化學 來源: 題型:
【題目】下列關于圖示如下圖的說法,正確的是
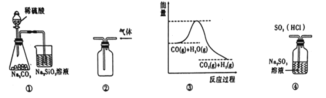
A.用圖①所示實驗可比較硫、碳、硅三種元素的非金屬性強弱
B.用圖②所示實驗裝置采用排空氣法收集已烯氣體
C.圖③表示可逆反應CO(g)+H2O(g)![]() CO2(g)+H2(g)的△H大于0
CO2(g)+H2(g)的△H大于0
D.圖④裝置可以用來除去SO2中的HCl
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在給定的條件下,下列選項所示的物質間轉化均能實現的是( )
A.SiO2![]() SiCl4
SiCl4![]() Si
Si
B.FeS2![]() SO2
SO2![]() H2SO4
H2SO4
C.N2![]() NH3
NH3![]() NH4Cl(aq)
NH4Cl(aq)
D.MgCO3![]() MgCl2(aq)
MgCl2(aq)![]() Mg
Mg
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學設計如下實驗方案,以分離KCl和BaCl2兩種固體混合物。試回答下列問題:
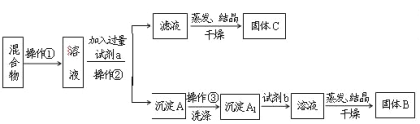
(1)操作①的名稱是_________。操作②的名稱是____________。
(2)試劑a是_________,試劑b是_________,固體B是________,固體C是________。
(3)加入試劑a所發生反應的離子方程式為:_________________________。
加入試劑b所發生反應的方程式為:____________________________。
(4)該方案能否達到實驗目的:_____________。若不能,應如何改進(若能,此問不用回答)? _____________________。
(5)若要測定原混合物中BaCl2的質量分數,除了要準確稱量混合物的質量外,至少還要獲得的數據是_____的質量。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某物質中元素被還原了,則該元素一定( )
①化合價升高 ②化合價降低 ③得到電子或電子對偏向 ④失去電子或電子對偏離
A.①② B.②④ C.②③ D.①④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法中錯誤的是
A.根據對角線規則,鈹和鋁的性質具有相似性
B.在H3O+、NH4+ 和[Cu(NH3)4]2+中都存在配位鍵
C.元素電負性越大的原子,吸引鍵合電子的能力越強
D.P4和CH4都是正四面體分子且鍵角都為109o28ˊ
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】.常溫下,將0.1 mol·L-1氫氧化鈉溶液與0.06 mol·L-1硫酸溶液等體積混合,該混合溶液的pH等于
A. 2.0 B. 1.7 C. 12.0 D. 12.4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對一定溫度下的恒容容器中的可逆反應A(g)+3B(g) ![]() 2C(g),下列敘述不能作為平衡標志的是
2C(g),下列敘述不能作為平衡標志的是
①C的生成速率與C的分解速率相等
②單位時間內生成amolA,同時生成3amolB
③A、B、C的濃度不再變化
④A、B、C的壓強不再變化
⑤混合氣體的總壓強不再變化
⑥混合氣體的物質的量不再變化
⑦單位時間內消耗amolA,同時生成3amolB
⑧A、B、C的分子數之比為1:3:2
A.②⑧ B.①⑥ C.②④ D.③⑧
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常見無機物A、B、C、D存在如圖轉化關系:

(1)若D是氯堿工業的主要產品,B有兩性氫氧化物,則反應②的離子方程式是: 。
(2)若A是一種堿性氣體,常用作制冷劑,B是汽車尾氣之一,遇空氣會變色,則反應①的化學方程式為 。
(3)若A為常見揮發性強酸,D是生產生活中用量最大用途最廣的金屬單質,,則B的化學式可能是 ,寫出反應②的離子方程式為 。
(4)若A、C、D都是常見氣體,C是形成酸雨的主要氣體,則反應③的化學方程式 。
(5)若A、B、C的水溶液均顯堿性,焰色反應均為黃色,D為CO2,用離子方程式解釋B溶液顯堿性的原因(用離子方程式表示)___________,舉出C的一種用途_______。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com