
Ո�㌑��һ�N��(sh��)�(y��n)����ȡ����Ļ��W(xu��)����(y��ng)����ʽ�� ��
Ո?ji��n)�����ăx���и���(j��)��������(y��ng)�x���m��(d��ng)?sh��)ăx���M��һ����ȡ���ռ������������b�ã�
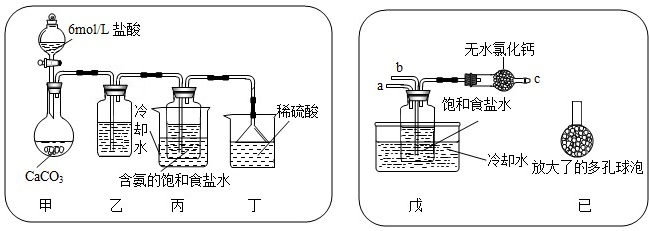
��1������(j��)�㌑�Ļ��W(xu��)����ʽ���㑪(y��ng)ԓ�x�����ȡ�b���� ��������̖��
��2�������b����D�b�õ������� ������E�b���ռ����⌧(d��o)��ܑ�(y��ng)�� �M(j��n)��
��3���C������ƿ�е������ѽ�(j��ng)�ռ��M�ķ�����_________________��
��4��ͨ�^����Y�ϵ�֪������(NH3)��һ�N�ܶȱȿ՚�С�ҘO������ˮ�Ě��w����ˮ��Һ�Q�鰱ˮ��С��ͬ�W(xu��)�ӟ��Ȼ��@�͚������}�Ĺ��w�������ȡ���⣬����(y��ng)�x��ķ���(y��ng)�İl(f��)���b���� __������ĸ��̖����С��ռ��M����ļ���ƿ�����ڵ��Пoɫ��̪��ˮ�У��^�쵽�ĬF(xi��n)�������������� �� ���� ����������
 ����Ӣ�Zϵ�д�
����Ӣ�Zϵ�д� ���ƌW(xu��)У�����ܜyϵ�д�
���ƌW(xu��)У�����ܜyϵ�д� �S������ȫ������(y��u)�yԇ��ϵ�д�
�S������ȫ������(y��u)�yԇ��ϵ�д�
| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M(f��i)�n�����]�� | ��һ | ��һ���M(f��i)�n�����]�� |
| �߶� | �߶����M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
| ���� | �������M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ���x����
| ||
| 106 |
| 100 |
| x |
| 10.00g |
| 10.6g |
| 13.25g |
| 106 |
| 100 |
| x |
| 10.00g |
| 10.6g |
| 13.25g |
| a |
| b |
| 53 |
| 22 |
| 53 |
| 22 |
| a |
| b |
| 53 |
| 22 |
| 53 |
| 22 |
| a |
| b |
| 53 |
| 22 |
| a |
| b |
| 53 |
| 22 |
| 53b |
| 22a |
| 53b |
| 22a |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
�҇��������Һ�°�ġ������ƉA�������������ƉA���I(y��)������ͻ��ؕ�I(xi��n)������NaCl��NH3 ��CO2�Ȟ�ԭ�����Ƶ�NaHCO3���M(j��n)�����a(ch��n)�����A�����P(gu��n)����(y��ng)�Ļ��W(xu��)����ʽ�飺NH3 + CO2 + H2O = NH4HCO3 �� NH4HCO3 + NaCl = NaHCO3��+ NH4Cl �� 2NaHCO3
Na2CO3 + CO2��+ H2O
��̼����@�c�ʳ�}ˮ����(y��ng)��������̼����c���w��ԭ���� �����(bi��o)̖����
A��̼����c�y����ˮ B��̼����c�ܟ��ֽ�
C��̼����c���ܽ�������^С����������Һ�����ȽY(ji��)������
��?ij̽�����С�M����(j��)�����ƉAԭ�����M(j��n)��̼����c���Ƃ䌍(sh��)�(y��n)��ͬ�W(xu��)���������O(sh��)Ӌ(j��)�ķ�����(sh��)�(y��n)��
�� һλͬ�W(xu��)��������̼?x��)��wͨ�뺬�����ʳ�}ˮ���Ƃ�̼����c����(sh��)�(y��n)�b�����D��ʾ���D�ЊA�֡��̶��õăx��δ��������
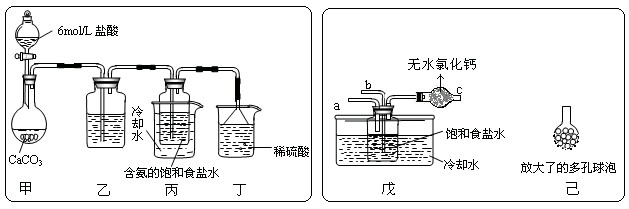
ԇ�ش��������P(gu��n)���}��
�������b���е�ԇ���� ��
�����b����ϡ����������� ��
����(sh��)�(y��n)�Y(ji��)�����x��NaHCO3 ���w�IJ����� ������x���������Q����
�� ��һλͬ�W(xu��)�ÈD�����b�ã������b��δ�������M(j��n)�Ќ�(sh��)�(y��n)��
����(sh��)�(y��n)�r(sh��)����ȏ� ��ͨ�� ���w���ُ� ����ͨ�� ���w��
������ͬ�W(xu��)���h�����b�õ�b���¶��B�Ӽ��b�ã�������
��
��?Ո���ٌ���һ�N��(sh��)�(y��n)����ȡ����̼����c�ķ�����
��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ��2011-2012�W(xu��)�꽭�Kʡ�(zh��n)���ГP(y��ng)���а��꼉���£����л��W(xu��)ԇ����4�·ݣ��������棩 �}�ͣ�����}
 Na2CO3+CO2��+H2O
Na2CO3+CO2��+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ��2011-2012�W(xu��)�꽭�Kʡ�(zh��n)���ГP(y��ng)���а��꼉���£����л��W(xu��)ԇ���������棩 �}�ͣ�����}
 Na2CO3+CO2��+H2O
Na2CO3+CO2��+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ��2012�꽭�Kʡ�(zh��n)���ГP(y��ng)�����п����W(xu��)ģ�Mԇ����4�·ݣ��������棩 �}�ͣ�����}
 Na2CO3+CO2��+H2O
Na2CO3+CO2��+H2O
�鿴�𰸺ͽ���>>
���H�W(xu��)У��(y��u)�x - ����(x��)���б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��(b��o)ƽ�_ | �W(w��ng)���к���Ϣ�e��(b��o)���^(q��) | ����p�_�e��(b��o)���^(q��) | ��vʷ̓�o���x�к���Ϣ�e��(b��o)���^(q��) | �����֙�(qu��n)�e��(b��o)���^(q��)
�`���Ͳ�����Ϣ�e��(b��o)�Ԓ��027-86699610 �e��(b��o)�]�䣺58377363@163.com