
【題目】下列應用,相關化學方程式及基本反應類型都正確的是( )
A. 一氧化碳用于煉鐵:4CO+Fe3O4![]() 3Fe+4CO2 置換反應
3Fe+4CO2 置換反應
B. 用氫氧化鈣溶液吸收二氧化碳氣體:Ca(OH)2+CO2=CaCO3↓+H2O 復分解反應
C. 用含有氫氧化鋁的藥物治療胃酸過多癥:Al(OH)3+3HCl=AlCl3+3H2O 復分解反應
D. 實驗室加熱高錳酸鉀制取氧氣:K2MnO4![]() 2KMnO4+MnO2+O2↑ 分解反應
2KMnO4+MnO2+O2↑ 分解反應
 金博士一點全通系列答案
金博士一點全通系列答案科目:初中化學 來源: 題型:
【題目】某校化學興趣小組參觀制堿廠后,獲得以下信息并對相關問題進行研究.
產品原理:該廠采用“侯氏制堿法”生產化工產品﹣﹣純堿(Na2CO3)和化肥NH4Cl.
生產原理是:將NH3和CO2通入飽和食鹽水中得到NaHCO3晶體和NH4Cl溶液,反應的化學方程式為:_____;后分離出NaHCO3,加熱制得純堿.
生產流程:
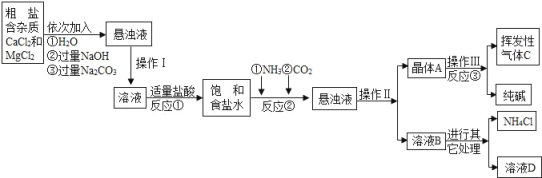
相關資料:
(1)NH4Cl ![]() NH3↑+HCl↑
NH3↑+HCl↑
(2)已知20℃時有關物質的溶解度如下(氣體指1體積水中能溶解的氣體體積)
物質 | NaCl | NaHCO3 | NH4Cl | NH3 | CO2 |
溶解度 | 36.0g | 9.6g | 37.2g | 710 | 0.9 |
問題討論:
(1)操作Ⅰ、Ⅱ中,相同操作的名稱為_____.反應①中發生了兩個反應,寫出其中一個化學方程式:_____,反應①加適量的鹽酸,適量是指_____.
(2)檢驗揮發性氣體C的方法_____.
(3)上述生產流程中可循環使用的是_____(填序號).
A揮發性氣體C; B溶液D; C氫氧化鎂;D化肥NH4Cl
組成確定:
(1)稱取一定質量的純堿樣品,經多次充分加熱后,再稱重,質量無變化;
(2)另取少量純堿樣品加入適量水,樣品完全溶解,向該溶液中加入過量稀HNO3,再滴加AgNO3溶液,有白色沉淀.由上述實驗可確定純堿樣品含有雜質_____(寫化學式).
含量測定:
實驗一 | 實驗二 | 實驗三 | 實驗四 | |
固體混合物溶液質量 | 100g | 100g | 100g | 100g |
加入CaCl2溶液質量 | 10g | 20g | 30g | 40g |
生成的沉淀的質量 | 4g | m | 10g | 10g |
稱取該純堿樣品44g固體混合物,加水配成400g溶液,平均分為四份,然后分別加入一定質量分數的CaCl2溶液,實驗數據見表:
請分析表中數據回答并計算:
(1)m=_____g;
(2)在實驗三中,完全反應后所得溶液中溶質氯化鈉的質量分數是多少?_____(要求寫計算過程,結果保留0.1%)
總結反思:
請通過計算并結合下表判斷此純堿樣品等級為_____品,在上述純堿含量測定中,將CaCl2溶液改為BaCl2溶液,測定誤差會減小.
工業純堿標準:(Na2CO3% ) | |||
優等品 | 一等品 | 合格品 | 次品 |
≥95 | ≥80 | ≥75 | ≤40 |
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】四種物質在一定條件下充分混合反應,測得反應前后各物質的質量分數如圖所示,則有關說法中正確的( )

A. 丙一定是化合物
B. 該反應可能是水的電解
C. 乙一定是該反應的催化劑
D. 參加反應或生成的甲和丙的質量比為19:41
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】甲、乙、丙三種固體物質的溶解度曲線如圖所示,請回答。
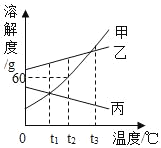
(1)溫度為_____℃時,甲、乙、丙三種物質的溶解度大小關系為乙>甲=丙。
(2)若甲中含有少量乙,可用_____的方法提純甲。
(3)t2℃時,在50g水中加入_____g甲物質,恰好形成飽和溶液。
(4)接近飽和的丙溶液,在保持溶質質量分數不變的情況下轉變為飽和溶液,可采取的方法是_____。
(5)將t3℃時,等質量的甲、乙、丙三種物質的飽和溶液,同時降溫到t1℃,所得溶液中溶質質量分數由大到小的順序是_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】t2℃時,將甲、乙各80g分別放到盛有100g水的兩個燒杯中,充分溶解后,恢復到t2℃,現象如圖,甲和乙的溶解度曲線如圖。請結合圖示回答下列問題:

(1)能說明固體甲對應的溶解度曲線是a的證據是_______。
(2)下列關于t2 ℃時,甲、乙所得溶液的說法不正確的是______(填序號)。
A 溶質質量:甲<乙 B 乙為飽和溶液
C 溶質質量分數:甲=乙 D 將溶液降溫至t1 ℃時,甲、乙的溶解度相等。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】九年級綜合實踐活動小組用過氧化氫溶液和二氧化錳來制取氧氣,最后所得到氣體質量與時間的關系如圖所示.
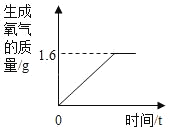
(1)過氧化氫中氧元素的化合價是_____價;
(2)反應生成氧氣的質量為_____g
(3)計算參加反應的過氧化氫的質量?_____(寫出計算過程)
查看答案和解析>>
科目:初中化學 來源: 題型:
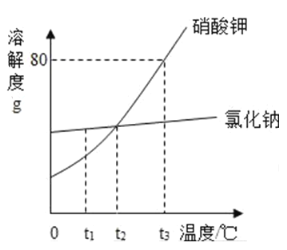
【題目】請根據如圖所示的溶解度曲線回答下列問題.
(1)t1℃時,硝酸鉀溶解度_____(選填“>”、“<”或“=”)氯化鈉的溶解度;
(2)若想使t2℃的硝酸鉀的不飽和溶液變成該溫度下的飽和溶液,最簡單的方法是_____;
(3)t3℃時將60g硝酸鉀溶液50g水中,所得溶液中溶質與溶劑的質量比為_____.
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】閱讀下面科普短文。
說起二氧化硫(SO2),你可能首先想到它是空氣質量播報中提及的大氣污染物。其實你真的了解SO2嗎?難道它只是有害物質嗎?
SO2與食品工業
SO2作為防腐劑、漂白劑和抗氧化劑廣泛用于食品行業。葡萄酒釀制中適量添加SO2,可防止葡萄酒在陳釀和貯藏過程中被氧化,抑制葡萄汁中微生物的活動。食糖加工過程中可使用SO2進行脫色。按照我國《食品添加劑使用標準(GB2760-2014)》,合理使用SO2不會對人體健康造成危害。
標準中部分食品SO2的最大殘留量
食品 | 蜜餞 | 葡萄酒 | 食糖 | 水果干 | 巧克力 | 果蔬汁 |
最大殘留量 | 0.35g/kg | 0.25g/L | 0.1g/kg | 0.1g/kg | 0.1g/kg | 0.05g/kg |
SO2與硫酸工業
硫酸是重要的化工原料,工業制硫酸的關鍵步驟是SO2的獲取和轉化。工業利用硫制硫酸的主要過程示意如下:
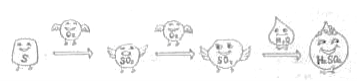
硫酸工業的尾氣中含有少量SO2,若直接排放會污染空氣,并導致硫酸型酸雨。工業上可先用氨水吸收,再用硫酸處理,將重新生成的SO2循環利用。
SO2與化石燃料
化石燃料中的煤通常含有硫元素,直接燃燒會產生SO2。為了減少煤燃燒產生的SO2污染空氣,可以采取“提高燃煤質量,改進燃燒技術”的措施,例如,對燃煤進行脫硫、固硫處理;還可以采取“優化能源結構、減少燃煤使用”的措施,例如,北京大力推廣的“煤改氣、煤改電”工程,有效改善了空氣質量。
現在,你對SO2一定有了新的認識,在今后的化學學習中你對SO2還會有更全面的認識!
依據文章內容回答下列問題。
(1)按照國家標準,食糖中的SO2最大殘留量為 g/kg。
(2)葡萄酒釀制過程中SO2的作用是 。
(3)用硫制硫酸的主要過程中,涉及到的含硫物質有S、 和H2SO4。
(4)硫酸工業生產中,吸收尾氣中SO2的物質是 。
(5)下列措施能減少SO2排放的是 (填序號)。
A.將煤塊粉碎 B.對燃煤進行脫硫
C.推廣煤改氣、煤改電 D.循環利用工業尾氣中的SO2
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】A、B、C、D、E、F、G、H八種物質,有下圖所示關系:其中A是一種暗紫色固體,B是黑色固體,D能使帶火星的木條復燃,E 、F都是無色液體,G是木炭,H是一種能使澄清石灰水變渾濁的氣體,在②的反應前后B的質量和化學性質都不改變。

請你根據上述信息,推斷出下列物質。
(1)填名稱:A 、B ,C 、H 。
(2)寫出反應③的化學方程式,并指出反應的基本類型:
③ ; 反應
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com