��2012?�P(y��ng)����ģ�M���҇��������Һ�°�ġ������ƉA�������������ƉA���I(y��)������ͻ��ؕ�I(xi��n)������NaCl��NH
3��CO
2�Ȟ�ԭ�����Ƶ�NaHCO
3���M(j��n)�����a(ch��n)�����A�����P(gu��n)����(y��ng)�Ļ��W(xu��)����ʽ�飺
NH
3+CO
2+H
2O�TNH
4HCO
3��
NH
4HCO
3+NaCl�TNaHCO
3��+NH
4Cl��
2NaHCO
3Na
2CO
3+CO
2��+H
2O
�ش����І��}��
��1��̼����@�c�ʳ�}ˮ����(y��ng)��������̼����c���w��ԭ����
c
c
������ĸ��(bi��o)̖����
a��̼����c�y����ˮ b��̼����c�ܟ��ֽ� c��̼����c���ܽ�������^С����������Һ�����ȽY(ji��)������
��2��ij̽�����С�M����(j��)�����ƉAԭ�����M(j��n)��̼����c���Ƃ䌍(sh��)�(y��n)��ͬ�W(xu��)���������O(sh��)Ӌ(j��)�ķ�����(sh��)�(y��n)��
��һλͬ�W(xu��)��������̼?x��)��wͨ�뺬�����ʳ�}ˮ���Ƃ�̼����c����(sh��)�(y��n)�b�����D��ʾ���D�ЊA�֡��̶��õăx��δ��������
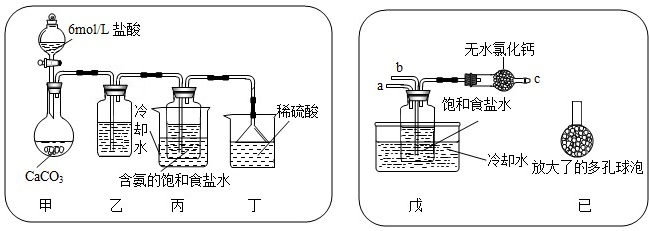
ԇ�ش��������P(gu��n)���}��
�������b���е�ԇ���� ͵�̼����c��Һ��������
���ռ��b�ÿ��ܓ]�l(f��)�����Ȼ�����w
���ռ��b�ÿ��ܓ]�l(f��)�����Ȼ�����w
��
�����b����ϡ�����������
����ĩ����(y��ng)��NH3
����ĩ����(y��ng)��NH3
��
����(sh��)�(y��n)�Y(ji��)�����x��NaHCO
3���w�IJ�����
�^�V
�^�V
������x���������Q����
����һλͬ�W(xu��)�ÈD�����b�ã������b��δ�������M(j��n)�Ќ�(sh��)�(y��n)��
����(sh��)�(y��n)�r(sh��)����ȏ�
a
a
��ͨ��
����
����
���w��
������ͬ�W(xu��)���h�����b�õ�b���¶��B�Ӽ��b�ã�������
������w�c��Һ���|��e�����CO2������
������w�c��Һ���|��e�����CO2������
��
��3��Ո���ٌ���һ�N��(sh��)�(y��n)����ȡ����̼����c�ķ�����
��̼����@�c�m���ʳ�}ˮ����(y��ng)�����������A��Һ��ͨ���^��CO2�����Na2CO3 ��Һ��ͨ���^��CO2 �ȣ����������������ɣ�
��̼����@�c�m���ʳ�}ˮ����(y��ng)�����������A��Һ��ͨ���^��CO2�����Na2CO3 ��Һ��ͨ���^��CO2 �ȣ����������������ɣ�
��
��4�������A�г��������������Ȼ��c����ij�о��ԌW(xu��)��(x��)С�M��һ�����A��ֻ���]���Ȼ��c�����о�����̽�����A��Ʒ��̼���c�ĺ�����
����(sh��)�(y��n)�O(sh��)Ӌ(j��)��
����
���O(sh��)Ӌ(j��)˼·������(j��)��Ʒ�c�Ȼ��}��Һ����(y��ng)���ɳ���̼���}���|(zh��)�������̼���c���|(zh��)������Ӌ(j��)���Ʒ��̼���c���|(zh��)����?j��n)?sh��)��
�������E���Qȡ13.25g���A��Ʒ�������^�����Ȼ��}��Һ�����?j��n)��裮�^�V��ϴ�졢����õ��İ�ɫ����10.00g��
��?d��ng)?sh��)��(j��)̎����Ո����(j��)������(sh��)�(y��n)��(sh��)��(j��)��Ӌ(j��)��ԓ��Ʒ��̼���c���|(zh��)����?j��n)?sh��)��
Ӌ(j��)���^�̣�
�⣺�O(sh��)���A��Ʒ�к�Na
2CO
3���|(zh��)����x
Na
2CO
3+CaCl
2�TCaCO
3��+2NaCl
106 100
x 10.00g
=x=10.6g
���A��Ʒ��Na
2CO
3���|(zh��)����?j��n)?sh��)��
��100%=80%
�⣺�O(sh��)���A��Ʒ�к�Na
2CO
3���|(zh��)����x
Na
2CO
3+CaCl
2�TCaCO
3��+2NaCl
106 100
x 10.00g
=x=10.6g
���A��Ʒ��Na
2CO
3���|(zh��)����?j��n)?sh��)��
��100%=80%
�ҷ���
I���O(sh��)Ӌ(j��)˼·������(j��)��Ʒ���|(zh��)����a g���cϡ������ȫ����(y��ng)���ɶ�����̼���|(zh��)�����|(zh��)����b g�������̼���c���|(zh��)������Ӌ(j��)���Ʒ��̼���c���|(zh��)����?j��n)?sh��)��
II����(sh��)�(y��n)�Y(ji��)Փ��
��1����(d��ng)a��b���|(zh��)���P(gu��n)ϵ�M��
�����a��b��ĸ�ı��_(d��)ʽ����ͬ���r(sh��)�����A��Ʒ��ֻ����̼���c����Ʒ��̼���c���|(zh��)����?j��n)?sh��)��100%��
��2����(d��ng)a��b���|(zh��)���P(gu��n)ϵ�M��
�r(sh��)�����A��Ʒ����̼���c�������Ȼ��c�M�ɵĻ�����Ʒ��̼���c���|(zh��)����?j��n)?sh��)��
��
����(sh��)�(y��n)�u�r(ji��)��
�`�������
��һ�������У���ɫ�������|(zh��)�����^�V������Ȳ����^���Е������p�ģ����Ӌ(j��)��Y(ji��)���c��(sh��)�Hֵ���ƫС��������Ȼ��}��Һ�Q���Ȼ��^��Һ���t����ʹ�`��pС��������
BaCl2��CaCl2�����������|(zh��)���a(ch��n)���ij����|(zh��)���Q���`��С
BaCl2��CaCl2�����������|(zh��)���a(ch��n)���ij����|(zh��)���Q���`��С
��
�������ҷ����У��в������ɵĶ�����̼?x��)��w���ܽ���ˮ���]��ȫ���ݳ������Ӌ(j��)��Y(ji��)���c��(sh��)�Hֵ���
ƫС
ƫС
���ƫ����ƫС������׃������





 Na2CO3+H2O+CO2����
Na2CO3+H2O+CO2����
 Na2CO3+CO2��+H2O
Na2CO3+CO2��+H2O
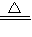 Na2CO3+H2O+CO2����
Na2CO3+H2O+CO2����