
(9分)火力發電廠用石灰石泥漿吸收廢氣中的二氧化硫以防止污染環境,其反應方程式為:
2CaCO3(粉末)+2SO2+O2==2CaSO4+2CO2。
(1)若100克廢氣中含6.4克二氧化硫,則處理100克這種廢氣需含碳酸鈣(CaCO3)80%的
石灰石多少克。
(2)處理上述100克廢氣,可得到含CaSO485%的粗產品多少克。
設需含CaCO380%的石灰石的質量為x,則含純物質CaCO3的質量為80%×x.又設生成純CaSO4質量為y.
2CaCO3+2SO2+O2═2CaSO4+2CO2
200 128 272
80%×x 6.4g y
6.4g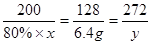 解得:x=12.5g y=13.6g
解得:x=12.5g y=13.6g
可得到含CaSO485%的粗產品的質量是: =16g
=16g
答:(1)需含碳酸鈣(CaCO3)80%的石灰石12.5克.
(2)處理上述100克廢氣,可得到含CaSO485%的粗產品16克.
解析試題分析:首先要明確在利用化學方程式進行計算用料和產量時,由于化學方程式表示的是純凈物質之間的質量關系,利用公式:純度= ×100%%,找到已知量和未知量.最后根據化學方程式計算的步驟、格式,結合著不純物質和純物質之間的相互轉化方法,列出比例式求解即可.
×100%%,找到已知量和未知量.最后根據化學方程式計算的步驟、格式,結合著不純物質和純物質之間的相互轉化方法,列出比例式求解即可.
考點:根據化學反應方程式的計算


科目:初中化學 來源: 題型:計算題
(5分)某化學興趣小組為了測定一工廠廢水中硫酸的質量分數,取100g廢水于燒杯中,加入80g質量分數為10%的氫氧化鈉溶液,恰好完全反應(廢水中無不溶物,其它成份不與氫氧化鈉反應)。試計算廢水中硫酸的質量分數。
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
將一定質量的氯化鈉和碳酸鈉的混合物加水溶解,再向此溶液中加入50g一定溶質質量分數的稀鹽酸,恰好完全反應.經數據分析可知放出氣體4.4g,經測定,濾液中含氯元素的質量21.3g(假定物質質量無損失).求:
(1)所加稀鹽酸的溶質質量分數.
(2)原固體混合物中氯化鈉的質量.
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
(3分)鈦(Ti)是廣泛應用于航空、航海等領域的一種重要金屬。在一定條件下,鈦由四氯化鈦(TiCl4)和金屬鎂反應而制得:TiCl4+2Mg==Ti+2MgCl2 。現有380kg四氯化鈦,計算可生產金屬鈦的質量。
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
為了測定未知濃度稀硫酸的溶質質量分數,取氫氧化鋇溶液15g,逐滴加入該待測稀硫酸,同時測定并記錄反應過程中混合溶液的pH變化情況(如圖所示),過濾后得到濾液32.67g.
求:(1)反應后生成硫酸鋇的質量是多少;
(2)該稀硫酸的溶質質量分數。
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
乙醇是一種清潔的綠色能源,可再生,俗稱酒精,其化學式為C2H5OH,其在空氣中完全燃燒的化學方程式為:C2H5OH+3O2 2CO2+3H2O,現有100g質量分數為92%的乙醇溶液在空氣中完全燃燒產生二氧化碳的質量為多少克?
2CO2+3H2O,現有100g質量分數為92%的乙醇溶液在空氣中完全燃燒產生二氧化碳的質量為多少克?
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
工業上用煅燒石灰石制備二氧化碳。現有含雜質10%的石灰石100 t(雜質不參與反應,且不含鈣元素),經高溫煅燒后,若測得剩余固體中鈣元素的質量分數為50%。
已知:CaCO3 CaO+CO2↑
CaO+CO2↑
通過計算回答:
(1)生成二氧化碳的質量。
(2)石灰石中的碳酸鈣是否完全分解。
查看答案和解析>>
科目:初中化學 來源: 題型:計算題
將100g氯化鉀樣品(含有碳酸鉀雜質)加入到50g鹽酸中,樣品完全反應,產生氣體全部逸出,得到145.6g溶液。請計算:
(1)產生氣體的質量為: g;
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com