
化學興趣小組的同學們探究用Fe從含Fe2(SO4)3和CuSO4的溶液中獲取金屬Cu的原理.請你一起參與探究.
(1)實驗依據:金屬活動順序.請在下表對應的方框內填入鐵和銅的元素符號.

(2)意外發現:小明將光亮的鐵絲插入含Fe2(SO4)3和CuSO4的廢液中,一段時間后取出,意外地發現鐵絲表面沒有變紅.
(3)提出問題:Fe為什么沒有從廢液中置換出Cu?
(4)提出假設:小麗認為在鐵絲表面可能有Cu析出,但被Fe2(SO4)3溶液溶解了.
(5)驗證假設:提供的主要實驗用品:潔凈的鐵絲和銅絲各兩根,相同體積、相同濃度的Fe2(SO4)3溶液三份[Fe2(SO4)3溶液顯黃色].
| 實驗操作 | 實驗現象和數據 | 結論 |
| ①準確稱量潔凈的鐵絲和銅絲的質量 | 鐵絲質量為ag, | \ |
| ②將鐵絲插入Fe2(SO4)3溶液中,一段時間后取出、洗凈、干燥、稱量 | 鐵絲質量為mg,(m<a),溶液有黃色變為淺綠色 | 一定有 生成(填化學式) |
| ③將銅絲插入Fe2(SO4)3溶液中,一段時間后取出、洗凈、干燥、稱量 | 銅絲質量為ng(n<b) | 銅 (填“能”或“不能”)與Fe2(SO4)3溶液反應 |
| ④另取相同質量、相同粗細的潔凈鐵絲和銅絲互相纏繞,插入Fe2(SO4)3溶液中,一段時間后取出、洗凈、干燥、分別稱量鐵絲和銅絲的質量 | 鐵絲質量較輕 | Fe、Cu共存時 優先與Fe2(SO4)3溶液反應 |
(6)實驗結論:小麗的假設 (選填“成立”或“不成立”),理由是 ;
(7)思考與交流:
①興趣小組的同學們通過對上述實驗的分析,找到了用Fe從含Fe2(SO4)3和CuSO4的溶液中提取金屬Cu的關鍵,并且最終實驗獲得了成功,其實驗成功的關鍵是: .并且反應充分.
②已知Fe和Fe2(SO4)3發生化合反應.請按反應順序寫出用Fe從含Fe2(SO4)3和CuSO4的溶液中獲取金屬Cu的化學方程式: ; .
試題分析:(1)熟記金屬活動性順序表,并會寫元素符號,故答案為:Fe Cu;
(5)②根據反應后鐵絲的質量減少了,并且溶液由黃色變為淺綠色,確定為硫酸亞鐵溶液,故答案為:FeSO4
③將銅絲插入Fe2(SO4)3溶液中,一段時間后取出、洗凈、干燥、稱量,銅絲質量為ng(n<b),銅能與Fe2(SO4)3溶液反應,故答案為:能;
④根據實驗后的現象“鐵絲質量較輕,銅絲質量不變”得知Fe、Cu共存時Fe優先與Fe2(SO4)3溶液反應,故答案為:Fe;
(6)用Fe從含Fe2(SO4)3和CuSO4的溶液中獲取金屬Cu,實驗過程Fe沒有從廢液中置換出Cu,小麗認為在鐵絲表面可能有Cu析出,但被Fe2(SO4)3溶液溶解了.但是根據實驗探究的結果發現Fe、Cu共存時Fe優先與Fe2(SO4)3溶液反應,所以小麗的假設錯誤的,故答案為:不成立;Fe、Cu共存時Fe優先與Fe2(SO4)3溶液反應;
(7)①根據實驗探究的結果,我們得知鐵先于硫酸鐵溶液反應生成硫酸亞鐵,所以只有加入過量的鐵才能發生鐵與硫酸銅溶液的置換反應,從而生成銅,故答案為:加入過量的鐵;
②已知Fe和Fe2(SO4)3發生化合反應,且生成的是淺綠色的溶液;鐵與硫酸銅溶液的反應屬于置換反應是教材上學過的反應方程式,故答案為:Fe+Fe2(SO4)3=3FeSO4 Fe+CuSO4=FeSO4+Cu


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:初中化學 來源: 題型:

查看答案和解析>>
科目:初中化學 來源: 題型:
| 實 驗 步 驟 | 實 驗 現 象 | 結 論 |
| 分別把這兩種金屬放入 稀鹽酸 稀鹽酸 溶液中,觀察. | 金屬Y表面無明顯變化;金屬X的表面有大量氣泡冒出.將燃著的木條放在金屬X的試管口,氣體燃燒. | 金屬活動性順序: X>Y X>Y |
查看答案和解析>>
科目:初中化學 來源: 題型:



查看答案和解析>>
科目:初中化學 來源: 題型:
查看答案和解析>>
科目:初中化學 來源: 題型:
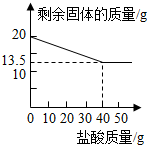 如今市場上出現的假黃金(銅鋅合金)坑害了許多消費者.某校化學興趣小組的同學們為測定假黃金的組成,稱取20克假黃金置于燒杯中,用某未知溶質質量分數的稀鹽酸50克,分5次加入,每次充分反應后,取出固體,經過濾、干燥等操作后稱重,各次稀鹽酸用量和剩余固體質量記錄如下:
如今市場上出現的假黃金(銅鋅合金)坑害了許多消費者.某校化學興趣小組的同學們為測定假黃金的組成,稱取20克假黃金置于燒杯中,用某未知溶質質量分數的稀鹽酸50克,分5次加入,每次充分反應后,取出固體,經過濾、干燥等操作后稱重,各次稀鹽酸用量和剩余固體質量記錄如下:| 實驗次數 | 稀鹽酸的用量(g) | 剩余固體的質量(g) |
| 1 | 10 | 18.375 |
| 2 | 10 | 16.750 |
| 3 | 10 | 15.125 |
| 4 | 10 | 13.500 |
| 5 | 10 | 13.500 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com