
下面是實驗室制取和收集氣體的裝置,請按要求作答:
某興趣小組利用下圖裝置探究制取氣體的原理、方法及性質。結合裝置圖,回答問題: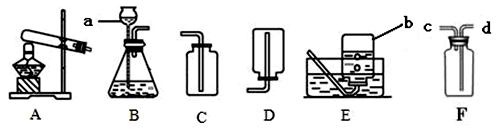
(1)寫出圖中標號儀器的名稱:a: ,b:
(2)實驗室準備用高錳酸鉀制取比較純凈的氧氣,采用的裝置組合是 ,該反應的化學方程式為 ;利用氯酸鉀和二氧化錳的混合物制取O2后的固體殘渣(假定已完全反應),通過以下四步實驗操作可回收二氧化錳。正確操作的先后順序是 (填寫選項序號)。
a.烘干 b.溶解 c.過濾 d.洗滌
(3)該小組想用B裝置來制取CO2,所用藥品名稱為 和 ;
該反應的化學方程式為 ;收集 CO2前,如果用F裝置中的某種溶液干燥CO2,則該溶液是 ;CO2應從F裝置的 端通入。
(4)該小組在制取CO2的時侯,發現二氧化碳收集好后,反應仍在發生,所以,他們想設計一個能隨時控制反應的發生與停止的裝置,你覺得右邊Ⅰ、Ⅱ、Ⅲ裝置中能實現上述意圖的是 。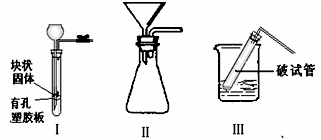
(1)長頸漏斗 集氣瓶(2)A、E 2KMnO4 加熱K2MnO4 + MnO2 + O2↑;bcda(3)大理石,稀鹽酸CaCO3 + 2HCl ="=" CaCl2 +H2O + CO2↑ (方程式3分,不寫“↑”扣1分,未配平扣1分,兩者都缺也只扣1分)濃硫酸 d (4)Ⅰ、Ⅲ
解析試題分析:(1)根據實驗室常用儀器回答,儀器a的名稱是長頸漏斗,b是集氣瓶。
(2)高錳酸鉀在加熱的條件下分解,生成錳酸鉀、二氧化錳和氧氣,故反應的化學方程式是2KMnO4 K2MnO4+ MnO2+O2↑;由此可知,實驗室用加熱高錳酸鉀固體分解制取氧氣的反應屬于“固體加熱型”,故發生裝置要選用A;由于氧氣的密度比空氣大,且不易溶于水,故可用向上排空氣法C或排水法E來收集,但根據題意,要收集比較純凈的氧氣,而排水法比排空氣法收集要純凈,故選排水法E。
K2MnO4+ MnO2+O2↑;由此可知,實驗室用加熱高錳酸鉀固體分解制取氧氣的反應屬于“固體加熱型”,故發生裝置要選用A;由于氧氣的密度比空氣大,且不易溶于水,故可用向上排空氣法C或排水法E來收集,但根據題意,要收集比較純凈的氧氣,而排水法比排空氣法收集要純凈,故選排水法E。
由于氯酸鉀在二氧化錳作催化劑的作用下,受熱分解生成氯化鉀和氧氣(逸出),故若已完全反應,則反應后的固體殘渣是生成的氯化鉀和二氧化錳(催化劑在反應前后不變)的混合物;其中氯化鉀易溶于水,二氧化錳不溶于水,故要回收二氧化錳,可先加水溶解,然后過濾,再將所得濾渣(二氧化錳)洗滌、干燥即可,故正確操作的先后順序是bcda。
(3)根據圖示,B裝置是固液常溫型裝置,實驗室一般選用塊狀大理石或石灰石和稀鹽酸反應,來制取二氧化碳,同時還生成氯化鈣和水,故反應的化學方程式為CaCO3+2HCl=CaCl2+CO2+H2O;由于濃硫酸具有吸水性,且不二氧化碳反應,故可用來干燥二氧化碳,如果用F裝置盛濃硫酸來干燥CO2,F就是洗氣瓶,則要長進短出,即CO2應從F裝置的長管d端通入。
(4)只要能實現固、液體兩種反應物的完全分離,就能隨時控制反應的發生與停止;裝置Ⅰ中的有孔塑料板可以放置固體,當關閉活塞時,由于裝置內氣體不能逸出,而使壓強增大,會將部分液體壓入長頸漏斗,使液面降至有孔隔板以下,由于固體留在了隔板上,故使固液體分離,從而導致反應停止;打開活塞時,氣體放出,壓強減小,液體再次進入并與固體接觸、反應;裝置Ⅱ中難以實現固液分離;裝置Ⅲ中的破了的試管恰好起到了與裝置Ⅰ中的有孔塑料板相同的作用,當試管移離燒杯,液體漏下,固液體即分離,當試管插入燒杯中液體中時,固液體即接觸反應。所以圖示裝置中只有Ⅰ、Ⅲ裝置能控制反應的發生與停止。
考點:常用儀器的名稱和選用,常用氣體的發生裝置和收集裝置與選取方法,實驗室制取氧氣的反應原理,實驗室制取二氧化碳的反應原理,書寫化學方程式
點評:熟記氧氣和二氧化碳的實驗室制法、原理和操作注意事項,是解題的關鍵;此外,本題的重點是常用氣體的發生裝置和收集裝置的選取方法,要學會根據反應物的狀態和反應的條件選擇發生裝置,根據制取氣體的溶解性和密度的大小選擇收集氣體的方法。


 閱讀快車系列答案
閱讀快車系列答案科目:初中化學 來源: 題型:

查看答案和解析>>
科目:初中化學 來源: 題型:閱讀理解
| ||
| △ |
| ||
| △ |
| ||
| ||
查看答案和解析>>
科目:初中化學 來源: 題型:
 如圖是實驗室用氯酸鉀制氧氣的裝置圖,請回答下列問題:
如圖是實驗室用氯酸鉀制氧氣的裝置圖,請回答下列問題:查看答案和解析>>
科目:初中化學 來源: 題型:解答題

查看答案和解析>>
科目:初中化學 來源:江蘇省期中題 題型:實驗題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com