
【題目】元素周期表是學習和研究化學的重要工具,我們可以從表中獲得許多知識。

(1)元素周期表中各周期結尾的元素是___________(填寫序號)。
A金屬元素 B非金屬元素 C稀有氣體元素
(2)如圖是元素周期表中一個方格內的部分內容,該元素的原子序數是______________,該元素的相對原子質量是___________,寫出該元素的單質在空氣中受熱的化學方程式______________。
(3)把銅片放到硝酸銀溶液中,會有銀白色固體析出。反應的化學方程式為________________。
科目:初中化學 來源: 題型:
【題目】閱讀下面科普短文。
酸奶營養豐富,富含人體生長發育所必須的多種營養物質,是人們喜愛的食品。
表 1 某品牌酸奶中主要營養成分的含量(每 100 克)
蛋白質/克 | 糖類/克 | 脂肪/克 | 鈉/毫克 | 鈣/毫克 |
2.7 | 9.5 | 2.7 | 75 | 90 |
但是,普通酸奶含有乳糖,經調查,我國有 88.9%的成人缺乏分解乳糖的乳糖酶,有55.1%的成年人表現有乳糖不耐受癥狀(主要癥狀為腹瀉)。因此,在保證普通酸奶基本營養不損失的前提下,乳糖含量較低或無乳糖的酸奶成為乳糖不耐受消費者的需求。相關科研技術人員為滿足消費者的需求,開始研發無乳糖酸奶。無乳糖酸奶的工藝流程為:原料乳 → 標準化 → 添加 6%的白砂糖 → 均質 → 巴氏殺菌 → 冷卻→接種發酵劑(直投式發酵劑)→ 發酵(37℃、42℃)→ 4℃低溫儲存。
研究一 發酵酸奶中添加乳糖酶對乳糖水解效果的影響
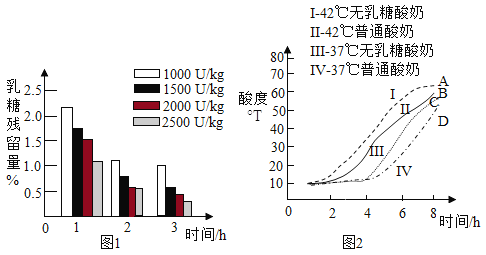
在 37℃,向普通酸奶中添加不同劑量乳糖酶(劑量分別為 1000U/kg、1500U/kg、2000U/kg、2500U/kg),發酵 3 小時,測得發酵酸奶中乳糖殘留量隨時間的變化,如圖 1 所示。
研究二 普通酸奶和無乳糖酸奶發酵過程中的酸度變化
普通酸奶和無乳糖酸奶分別在 37℃和 42℃發酵 8 小時,發酵過程中酸度(從 1 小時開始測量)變化如圖 2 所示。
除以上研究,科技人員還在口味、活菌數、保存等方面做了無乳糖酸奶與普通酸奶的對比研究,發現無乳糖酸奶都具有一定的優勢。
依據文章內容回答下列問題。
(1)由表 1 可知酸奶的主要營養成分中含量最高的是_______。
(2)由圖 1 可知:3 小時內,_______(填字母序號,下同)。
A添加相同量乳糖酶,發酵酸奶中乳糖殘留量隨時間的延長而降低
B相同發酵時間,乳糖殘留量均隨乳糖酶添加量的增大而降低
C乳糖殘留量與溫度、時間、乳糖酶添加量有關
(3)由圖 2,影響無乳糖酸奶酸度的因素是_______。
(4)由圖 2 可知:42℃時無乳糖酸奶發酵過程中酸度與時間的關系是_______。
(5)下列說法正確的是_______。
A我國絕大部分成年人都有乳糖不耐受癥狀
B表 1 中“鈉”指的是鈉元素
C無乳糖酸奶的工藝中至少兩步屬于化學變化
D無乳糖酸奶比普通酸奶適合更多消費者食用
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】苯甲酸鈉(C7H5O2Na)是一種食品添加劑,廣泛用于食品工業中,請計算:
(1)C7H5O2Na是由__________種原子構成; C7H5O2Na 的相對分子質量是_____;
(2)C7H5O2Na中碳、氧兩種元素的質量比是_______________。
(3)14.4g苯甲酸鈉中含有鈉元素____g。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】化學與人類生活密切相關。

(1)圖1中下列食物中,能提供大量維生素的是_____(填字母序號)。
(2)加碘鹽中“碘”是指_____(填“元素”或“分子”),身體一旦缺碘,可能患有的疾病是_____(填“甲狀腺腫大”或“骨質疏松”)。
(3)廚房中能用來除水垢的物質是_____(填“食醋”或“食鹽水”)。
(4)廚房中的下列物質在水中能形成溶液的是_____(填字母序號)。
A 調和油 B 食鹽 C 面粉 D 白糖
(5)洗滌餐具時加入少量洗滌劑,會有很好的洗滌效果,原因是洗滌劑可以起到_____作用。
(6)冬天常在汽車的水箱中加入少量乙二醇之類的化合物可以防止水箱中的水結冰,因為乙二醇溶于水后使溶液的凝固點_____(填“升高”或“降低”)。
(7)如圖2所示的“火立熄”是一種新型的家用滅火用品。“火立熄”接觸到火焰![]() 秒后炸開,釋放的粉末覆蓋在燃燒物上,同時放出不可燃氣體,使火焰熄滅。“火立熄”的滅火原理是_____(填字母序號)。
秒后炸開,釋放的粉末覆蓋在燃燒物上,同時放出不可燃氣體,使火焰熄滅。“火立熄”的滅火原理是_____(填字母序號)。
A 清除可燃物 B 使燃燒物與氧氣隔絕 C 降低燃燒物的著火點
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】為了測定一瓶硫酸銅溶液的溶質質量分數,取出50克該溶液,向其中逐滴加入溶質質量分數為16%的氫氧化鈉溶液,反應過程中生成沉淀的質量與所用氫氧化鈉溶液質量的關系如圖所示:
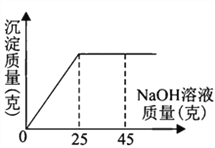
請你仔細分析此關系圖,并進行計算。
(1)當滴入氫氧化鈉溶液_____克時,硫酸銅與氫氧化鈉恰好完全反應。
(2)計算此硫酸銅溶液中溶質的質量分數為_________(寫出計算過程)。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】為測定某CuSO4溶液中溶質的質量分數,取150g CuSO4溶液,平均分為三份,每份樣品均按如圖所示進行實驗,實驗數據見下表。請計算:
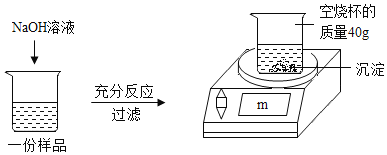
實驗1 | 實驗2 | 實驗3 | |
樣品質量/g | 50 | 50 | 50 |
NaOH溶液質量/g | 20 | 40 | 60 |
m/g | 42.45 | 44.9 | 44.9 |
(1)50g CuSO4溶液完全反應時,所得沉淀的質星為_____g。
(2)CuSO4溶液中溶質的質量分數為_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】在抗擊新型冠狀病毒肺炎戰役中做好殺菌消毒工作至關重要。下面是幾種常見的消毒劑:
(一)酒精(C2H5OH)
(1)在配制 75%的醫用酒精溶液時發現 75mL 的酒精和 25mL 的水混合后體積小于 100mL,其原因是________;
(2)在室內使用酒精消毒劑時,遇到明火易發生燃燒甚至爆炸。從燃燒的條件分析,明火的作用是______,酒精完全燃燒的化學方程式是______。
(二)過氧乙酸溶液 其標簽上的部分文字如圖。

(1)從標簽上的成分信息可以推知,過氧乙酸溶液受熱時容易發生_____;
(2)一瓶這種溶液中含溶質過氧乙酸_____g;
(3)過氧乙酸中碳、氫、氧元素的質量比為________________(填最簡整數比);
(4)新區實驗初中的校醫每天都用溶質質量分數為0.5%的過 氧乙酸溶液對教室等場所進行消毒。要配制這種溶液 600kg,需要溶質質量分數為 40%的過氧乙酸溶液____________kg。
(三)二氧化氯(ClO2)
資料:①ClO2是一種黃綠色、有刺激性氣味的氣體,熔點:﹣59.0℃,沸點:11.0℃,②冷卻至11.0℃以下時變成紅色液體,③易溶于水,④見光易分解,⑤易與堿反應,⑥殺菌、漂白能力均優 于 Cl2。消毒水體時不生成有害物質,也不存在用氯氣消毒時殘留的臭味。
(1)以上關于 ClO2 的描述中,屬于化學性質的是________________(填序號);
(2)制取 ClO2 的方法有多種,目前歐洲一些國家用氯酸鈉(NaClO3)與濃鹽酸反應制取 ClO2(Kestiog 法),同時有 Cl2、NaCl 和一種常見的氧化物生成,該反應中涉及的氯元素的化合價有________種;
(3)我國最近研究成功用 Cl2 和 NaClO2(N2 保護下)制取 ClO2,同時有 NaCl 生成,該反應的化學方程式是_____________;此法與 Kestiog 法相比,其優點是_________; (寫出其中的一條)
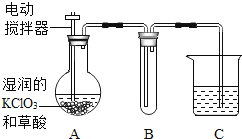
(4)工業上也可以在 60℃時,用稍加潮濕的 KClO3 與草酸(C2H2O4)反應制取 ClO2。某實驗小組用如下圖裝置制取并收集 ClO2,A 為 ClO2 的發生裝置,B 為 ClO2 的收集裝置,C 為尾氣吸收裝置。
請問:為了保證實驗成功,實驗時,A 裝置應浸在_____中加熱; B 裝置外加冰水冷卻,試管內可觀察到的現象是________;C 中所盛放的藥品可以是______。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】甲、乙、丙三種固體物質的溶解度曲線如圖所示,下列說法正確的是( )
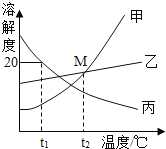
A. t1℃時,三種固體物質的溶解度大小的順序是丙>乙>甲
B. 升高溫度時,甲、乙、丙三種固體物質的不飽和溶液都能變成飽和溶液
C. t2℃時,將甲、乙兩物質的飽和溶液從t2℃降到t1℃,析出溶質質量甲>乙
D. t1℃時,將20g的丙物質溶入50g的水中,所得溶液溶質質量分數為20%
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】現有以下儀器,請回答下列問題:
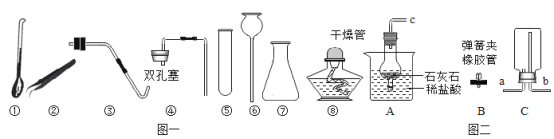
(1) 圖一中,取用粉末狀固體必須用到的儀器是__________________________ (填名稱,下同),儀器⑥是____ 。
(2)圖一中,若用過氧化氫溶液制取氧氣,發生裝置應選的儀器是_________________________(填序號),寫出鎂條在空氣中燃燒的現象:________________________。
(3)圖二中,A裝置中反應的化學方程式為_________________________;裝置A與B組合后具有的優點是________________________,收集氣體時導管c應該與導管_________________________(填“a”或“b”)相連接。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com