
“分解過氧化氫制氧氣的反應中二氧化錳的催化作用”,以及“尋找新的催化劑”研究性實驗,引起了化學探究小組的興趣。
【實驗探究一】氧化鐵能否作過氧化氫溶液分解的催化劑?如果能,催化效果如何?
| 實驗步驟 | 實驗現象 |
| I.分別量取5mL5%過氧化氫溶液放入A、B 兩支試管中,向A試管中加入ag氧化鐵粉末,并分別在A、B兩支試管中插入帶火星木條,觀察現象。 | A試管中產生氣泡,帶火星木條復燃,B試管中無明顯現象 |
| II.待A試管中沒有現象發生時,重新加入過氧化氫溶液,并把帶火星的木條伸入試管,如此反復多次試驗,觀察現象。 | 試管中均產生氣泡,帶火星木條均復燃 |
| III.將實驗II中的剩余物小心過濾,并將所得濾渣進行洗滌、干燥、稱量,所得固體質量仍為ag。 | |
| IV分別量取5mL5%過氧化氫溶液放入C、D 兩支試管中,向C試管中加入ag氧化鐵粉末,向D試管中加入ag二氧化錳粉末,觀察現象。 | |
| 實驗序號 | H2O2溶 液濃度% | H2O2溶液體積/mL | 溫度℃ | MnO2的用量/g | 收集氧氣的體積/mL | 反應所需 的時間/s |
| ① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| ② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| ③ | 30 | 5 | 35 | 0 | 2 | 49.21 |
| ④ | 30 | 5 | 55 | 0 | 2 | 10.76 |
(1)氧化鐵能加快過氧化氫分解的反應速率
(2)化學性質 質量
(3)H2O2  H2O + O2
H2O + O2
(4)二氧化錳催化效果比氧化鐵好
(5)反應物濃度(或濃度)③和④溫度越高,化學反應速率越快
(6)反應物濃度越大,單位體積的反應物中含有的粒子數越多,粒子間碰撞的概率越大,化學反應速率越快
解析試題分析:(1)通過對比實驗,說明氧化鐵確實改變了過氧化氫分解的速率。
(2)實驗Ⅱ說明氧化鐵仍能對過氧化氫的分解起加快作用,說明其化學性質沒有發生改變。實驗Ⅲ通過兩次稱量,說明其質量在反應前后并沒有發生改變。
(3)這個反應和二氧化錳作催化劑時的反應一樣,只需將催化劑由二氧化錳轉換成氧化鐵即可。反應的化符號表達式為:H2O2 H2O + O2
H2O + O2
(4)由于D試管中用的是二氧化錳,若實驗IV觀察到D試管中產生氣泡的速率更快,可以得到的結論是二氧化錳催化效果比氧化鐵好。
(5)實驗①和②中唯一的不同是過氧化氫溶液的濃度,所以我們可以得出反應速率還與反應物的濃度有關。要得出化學反應速率與溫度的關系,只需找到溫度不同而其他條件完全相同的兩個實驗作對比,觀察表格,容易發現實驗③和④符合我們的要求,且它們之間的關系是:溫度越高,化學反應速率越快。
(6)根據題目信息“化學反應的實質是微觀粒子相互接觸、碰撞的結果”,不難理解得出:反應物濃度越大,單位體積的反應物中含有的粒子數越多,粒子間碰撞的概率越大,化學反應速率越快。
考點:催化劑概念的理解,化學反應速率影響因素的探究


 優百分課時互動系列答案
優百分課時互動系列答案科目:初中化學 來源: 題型:探究題
實驗室里,試劑瓶的標簽常因脫落或被腐蝕而丟失,現有失去標簽的6瓶溶液,可能是NaCl、Na2CO3、NaOH、CaCl2、Ca(OH)2、HCl、CuSO4七種物質中的六種,教師將它們編號為A、B、C、D、E、F,讓同學們鑒別這六種物質,請你參與小明的下列鑒別過程.
[查閱資料]:CaCl2溶液顯中性,CaCl2+Na2CO3=CaCO3↓+2NaCl
(1)觀察各種溶液的顏色,其中C瓶為 色,是硫酸銅溶液.
(2)做兩兩混合實驗,E與其他四種物質混合的實驗現象記錄如下:
| | A | B | D | F |
| E | 無現象 | 白色沉淀 | 無色氣泡 | 白色沉淀 |
| 實驗操作 | 實驗現象及實驗結論 |
| | |
查看答案和解析>>
科目:初中化學 來源: 題型:探究題
小紅為大家做了一個“燃紙成鐵”的趣味實驗。將一張濾紙(組成元素為C、H、O)用FeCl3 濃溶液潤濕,在酒精燈上烘干后點燃,濾紙變黑、紅熱,最終生成黑褐色物質。小紅告訴大家:黑褐色物質中含有鐵單質。
【提出問題】黑褐色物質中真的含有鐵單質嗎?
【探究過程】
(1)小紅先從反應物組成分析,因為 所以反應后可能生成鐵單質。
(2)為獲得實驗證據,小紅做了實驗1。
實驗1:將黑褐色物質放入稀鹽酸中,發現有連續微小氣泡產生。若黑褐色物質中
含有鐵單質,則反應的化學方程式為 。
(3)小明提出疑問:實驗1中產生的氣泡也可能是濾紙碳化后吸附的空氣。為此,小紅又做了實驗2: 觀察到有微小氣泡產生但很快停止。
證明實驗1中的連續氣泡確實是由鐵單質與稀鹽酸反應產生的。
(4)為進一步證明黑褐色物質中有鐵單質,小紅又做了實驗3。
實驗3:將黑褐色物質放入 溶液中,觀察到紅色物質生成。
【得出結論】通過以上實驗探究,證明黑褐色物質中確實含有鐵單質。
(5)【實驗反思】小紅所做實驗1和實驗2是運用了 實驗,使結論更有說服力。
查看答案和解析>>
科目:初中化學 來源: 題型:探究題
鐵暴露在空氣中會生銹。不知你注意了沒有,將蘋果切開不久,果肉上就會產生一層咖啡色的物質,也好象是生了“銹”一樣。某化學活動小組對此進行了探究。
【提出問題】切開的蘋果“生銹”與什么因素有關?
【猜想與假設】
猜想①:可能是果肉中的物質與空氣中的氮氣作用而“生銹”;
猜想②:可能是果肉中的物質與空氣中的氧氣作用而“生銹”;
猜想③:可能是果肉中的物質與空氣中的二氧化碳作用而“生銹”;
【收集證據】
(一)查閱有關資料:已知蘋果“生銹”是果肉里的物質(酚和酶)與空氣中的一種物質發生氧化反應,生成咖啡色的物質。且溫度越高反應越快。
(二)實驗探究:針對上面的猜想,化學活動小組依次設計了實驗方案,將蘋果肉分別放入 三種氣體中,依次觀察到下列實驗現象。請你幫他們填寫下表。
| | 氮氣 | 氧氣 | 二氧化碳 |
| 現象 | 不變色 | 變色 | |
| 結論 | 果肉變色與氮氣無關 | | 果肉變色與二氧化碳無關 |
查看答案和解析>>
科目:初中化學 來源: 題型:探究題
某化學興趣小組同學為了研究影響分子運動速率的因素,如下圖所示,玻璃管左、右兩端分別放有脫脂棉,注射器中分別裝有濃鹽酸和濃氨水。濃氨水揮發出來的氨氣(NH3)和濃鹽酸揮發出來的氯化氫(HCl)能發生如下反應,NH3+ HCl=NH4Cl。兩個注射器同時向脫脂棉靠]近里邊的部位注入等體積的液體,過一會,先在A處產生大量白煙,然后白煙逐漸充滿整個試管。
根據現象回答問題:
(1)生成物NH4Cl常溫下的狀態是 (填“固體”、“液體”或“氣體”);
(2)有同學認為先在A處產生白煙是因為HCl分子比NH3分子運動速度慢,請你分析影響分子運動速度的因素可能是 ;
(3)影響分子運動速率的因素還有溫度,請舉出生活中的一個實例 ;
(4)該實驗中的注射器也可改用膠頭滴管直接滴入液體,相比較用注射器的優點是 。
查看答案和解析>>
科目:初中化學 來源: 題型:探究題
某化學小組同學利用如圖所示裝置進行實驗.
(1)若裝置Ⅰ中加入石灰石和過量稀鹽酸,裝置Ⅱ中加入澄清石灰水.打開a,關閉b,裝置Ⅰ中觀察到的現象是 ;一段時間后,關閉a,打開b,裝置Ⅱ中觀察到的現象是 .
(2)若利用裝置Ⅱ完成模擬合成氨氣(N2+3H2 2NH3)過程中的氣體混合實驗.從裝置Ⅱ右側導管通入氮氣,左側導管通入氫氣,則裝置Ⅰ中加入的藥品是 ,裝置Ⅱ中加入濃硫酸,則裝置Ⅱ的作用有:① ;②使氮氣和氫氣充分混合;③通過觀察 來控制氣體的體積比,從而提高氮氣和氫氣的利用率.
2NH3)過程中的氣體混合實驗.從裝置Ⅱ右側導管通入氮氣,左側導管通入氫氣,則裝置Ⅰ中加入的藥品是 ,裝置Ⅱ中加入濃硫酸,則裝置Ⅱ的作用有:① ;②使氮氣和氫氣充分混合;③通過觀察 來控制氣體的體積比,從而提高氮氣和氫氣的利用率.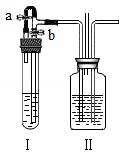
查看答案和解析>>
科目:初中化學 來源: 題型:探究題
張麗同學欲通過實驗證明“二氧化錳是過氧化氫分解的催化劑”這一命題。她設計并完成了下表所示的探究實驗:
| | 實驗操作 | 實驗現象 | 實驗結論或總結 | |
| 結論 | 總結 | |||
| 實驗一 | 取5mL5%的過氧化氫溶液于試管中,伸入帶火星的木條 | 有氣泡產生,木條不復燃 | 過氧化氫分解產生氧氣,但反應速率 。 反應的化學方程式為: 。 | 二氧化錳是過氧化氫分解的催化劑 |
| 實驗二 | 向盛水的試管中加入二氧化錳,伸入帶火星的木條 | 沒有明顯現象 | | |
| 實驗三 | | | 二氧化錳能加快過氧化氫的分解 | |
查看答案和解析>>
科目:初中化學 來源: 題型:探究題
某研究性學習小組將實驗室制備二氧化碳氣體反應后的廢物進行處理,目的是制取中性干燥劑CaCl2。得到固體后,他們對固體的成分進行了如下探究:
[提出猜想]
猜想一:只有CaCl2;
猜想二:CaCl2和CaCO3;
猜想三:CaCl2和HCl。
| | 操作 | 現象 | 結論 |
| 步驟一 |  | | 猜想二成立 |
| 步驟二 |  | |
查看答案和解析>>
科目:初中化學 來源: 題型:探究題
幾年前,一輛載滿20t電石的掛車,在浙江濱江區燃起熊熊大火并伴有大量黑煙.事故路面上灑落了五六百米燃著的石頭.這輛貨車在雨中整整燃燒了一天,消防官兵對大火也束手無措,場面讓人震撼.大家對電石的化學性質產生了濃厚的興趣,請你一起與他們完成下列探究活動.
【查閱資料】電石的主要成分是碳化鈣(CaC2),可以與水反應生成一種可燃性氣體及白色固體.常見的可燃性氣體中,乙炔(C2H2)燃燒時伴有大量黑煙.
【猜想與假設】
電石與水反應生成的可燃性氣體是:氧氣、氫氣或乙炔(C2H2);電石與水反應生成的白色固體是:氧化鈣、氫氧化鈣或碳酸鈣.大家做出以上推斷的理由是 .
大家討論后一致認為該氣體不可能是氧氣,原因是 ,白色固體不可能是氧化鈣,原因是(用化學方程式表示) .
【實驗探究】
| 實驗步驟 | 實驗現象 | 實驗結論 |
| (1)取適量電石加水反應,收集生成的氣體,驗純后點燃. | 氣體燃燒,產生黃色火焰并伴有濃烈黑煙. | 電石與水反應產生的氣體是 |
| (2)取適量反應后生成的固體于試管中,滴加過量稀鹽酸. | 固體溶解, . | 電石與水反應產生的固體不是碳酸鈣 |
| (3)取適量反應后生成的固體于試管中加水,向上層清液中滴加2~3滴 . | 溶液變紅 | 電石與水反應產生的固體是氫氧化鈣 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com